Р Е В М А Т О Л О Г И Я
Сухих Екатерина Николаевна
ПРИМЕНЕНИЕ ПРОСПИДИНА В
ТЕРАПИИ
АНКИЛОЗИРУЮЩЕГО
СПОНДИЛОАРТРИТА
14.00.39 – ревматология
АВТОРЕФЕРАТ
диссертации на соискание
ученой степени
кандидата медицинских наук
Ярославль – 2005
Работа выполнена в государственном
образовательном учреждении высшего профессионального образования «Кировская
Государственная медицинская академия Федерального агентства по здравоохранению
и социальному развитию Российской Федерации»
|
Научный руководитель |
доктор медицинских наук, профессор Немцов Борис Федорович |
|
Официальные оппоненты: |
доктор медицинских наук, профессор
Коршунов Николай Иванович |
|
|
доктор медицинских наук,
Сатыбалдыев Азамат Махмудович
|
Ведущая организация – Волгоградский государственный медицинский университет
Защита состоится «21» июня 2005г. в 12 час на заседании диссертационного совета
Д 208.119.01 при ГОУ ВПО «Ярославская государственная медицинская академия
Минздрава России» (150000, г. Ярославль, ул. Революционная 5)
С диссертацией можно ознакомится в библиотеке Ярославской государственной
медицинской академии
Автореферат разослан « » мая 2005
Ученый секретарь
Диссертационного
Совета
А.А. Зотов
Актуальность проблемы.
Анкилозирующий спондилоартрит – хроническое воспалительное заболевание с
поражением периферических суставов и позвоночника, приводящее в процессе
прогрессирования к анкилозированию и потере функциональной активности больных [Brandt
J.,
Braun J.,
2003]. Распространение анкилозирующего спондилоартрита в различных странах
составляет 0,5 – 2% в популяции, в России – 0,4% [Э.Р. Агабабова, 2002].
Анкилозирующий спондилоартрит в настоящее время занимает одно из ведущих мест в
ряду ревматической патологии по высоким темпам прогрессирования патологического
процесса и ранней инвалидизации больных; развивается в возрасте 15 – 30 лет,
однако 8,5% больных заболевают в возрасте 10 – 15 лет [Braun
J.,
Khan M.A.,
2003]. Отсутствие надежных диагностических критериев, неясность этиологии и
многих вопросов патогенеза являются причинами неудовлетворительных результатов
лечения анкилозирующего спондилоартрита [Sieper
J.,
Braun J.,
2002]. Поэтому анкилозирующий спондилоартрит привлекает внимание специалистов в
силу своей социальной значимости, отражая проблему необходимости ранней
диагностики, и разработки рациональных подходов к терапии, позволяющих
замедлить прогрессирование заболевания и сохранить функциональную активность и
трудоспособность больных. [О.М. Фоломеева, 2004,
Braun J.,
2003].
Симптоматическая терапия (НПВС, ГКС) занимает
ведущее положение в терапии анкилозирующего спондилоартрита, однако она
недостаточно эффективна для подавления активности и замедления прогрессирования
заболевания. Базисная терапия при анкилозирующем спондилоартрите менее
разработана, чем при других ревматических заболеваниях, а оценка ее
эффективности во многом затруднена вследствие выраженной гетерогенности болезни
[В.В.Бадокин, 2004]. В настоящее время из базисных препаратов при анкилозирующем
спондилоартрите в основном применяются сульфасалазин [Я.А.Сигидин, 2001,
Taylor A.,
2000], который более эффективен при периферической форме заболевания с высокой
лабораторной активностью, и метотрексат, отношение клиницистов к которому
неоднозначно [Biasi D.,
Sampai-Barros
P., 2000]. В последние 4 года были
опубликованы результаты ряда исследований, которые показали, что блокада ФНО-а
является очень эффективным методом лечения анкилозирующего спондилоартрита.
Однако необходимы дополнительные данные об их безопасности и способности
задерживать прогрессирование заболевания [Е.Л. Насонов, 2004].
По данным открытых
контролируемых исследований проспидин обладает клиническим эффектом при
ревматоидном и псориатическом артритах. В связи с этим, учитывая общие механизмы
воспалительных процессов при данных заболеваниях и анкилозирующем
спондилоартрите, представляется перспективным изучение клинической эффективности
проспидина при анкилозирующем спондилоартрите, включая открытое, контролируемое
исследование и сравнительный анализ с известными базисными препаратами и
нестероидными противовоспалительными средствами. Эти предпосылки и послужили
теоретическим обоснованием к проведению нашего исследования.
ЦЕЛЬ РАБОТЫ:
Обоснование клинической эффективности терапии проспидином при анкилозирующем
спондилоартрите в открытом контролируемом исследовании в сравнении с
метотрексатом.
ЗАДАЧИ РАБОТЫ
1.
Изучить клиническую эффективность терапии проспидином при анкилозирующем
спондилоартрите по ее влиянию на клинические проявления болезни и суточную
потребность в НПВС.
2. Оценить влияние терапии проспидином на
показатели функционального статуса и качества жизни больных анкилозирующим
спондилоартритом.
3. Выявить влияние терапии проспидином на некоторые лабораторные и
иммунологические параметры болезни.
4. Проанализировать характер и частоту побочных
действий терапии проспидином.
5. Провести сравнительный анализ клинической
эффективности проспидина, метотрексата и НПВС в терапии анкилозирующего
спондилоартрита.
6. Определить клиническое значение показателей
стабильных метаболитов оксида азота при анкилозирующем спондилоартрите.
7. Разработать методику
рациональной терапии проспидином при анкилозирующем спондилоартрите.
НАУЧНАЯ НОВИЗНА
Впервые изучена
клиническая эффективность терапии проспидином при анкилозирующем
спондилоартрите, влияние на клинические и лабораторные проявления заболевания,
характер и частота побочных действий. Выявлено влияние терапии проспидином на
иммунологические параметры болезни. Изучено влияние терапии проспидином на
качество жизни и функциональные возможности больных анкилозирующим
спондилоартритом. Впервые проведен сравнительный анализ клинической
эффективности проспидина с метотрексатом и НПВС при анкилозирующем
спондилоартрите. Проведено изучение клинического значения показателей стабильных
метаболитов оксида азота при анкилозирующем спондилоартрите.
ПРАКТИЧЕСКОЕ ЗНАЧЕНИЕ РАБОТЫ
Разработана рациональная методика применения
терапии проспидином при анкилозирующем спондилоартрите, критерии (клинические,
лабораторные, иммунологические) для ее назначения и контроля за ее
эффективностью, включающая: 1) выбор дозы и интервал введения препарата в
условиях стационара и на амбулаторном этапе; 2) показания и противопоказания к
ее применению; 3) критерии для назначения лечения и контроля за его
эффективностью и выявления возможных побочных действий. Показано, что применение
проспидина расширяет возможности базисной терапии при анкилозирующем
спондилоартрите.
ОСНОВНЫЕ ПОЛОЖЕНИЯ, ВЫНОСИМЫЕ НА ЗАЩИТУ
1.
Проспидин обладает клинической эффективностью при анкилозирующем
спондилоартрите, позволяет подавлять активность болезни уже на ранних этапах
лечения, оказывает положительное влияние на функциональную активность больных, а
также улучшает качество жизни.
2.
Терапия проспидином оказывает положительное влияние на некоторые
лабораторные и иммунологические показатели болезни.
3.
Побочные действия проспидина (36,3% случаев) в процессе терапии являются
в основном доброкачественными и обратимыми.
4.
Клиническая эффективность проспидина, оцененная по отдаленным результатам
лечения, превосходит клиническую эффективность НПВС и метотрексата.
5.
Определение стабильных метаболитов оксида азота сыворотки крови и мочи у
больных анкилозирующим спондилоартритом имеет диагностическое, при оценке
степени активности заболевания, и прогностическое (при оценке результатов
терапии) значение.
ПУБЛИКАЦИИ И АПРОБАЦИЯ РАБОТЫ.
По теме диссертации опубликовано 10 работ, из
них 4 в центральной, 1 в зарубежной печати.
Основные положения
диссертации доложены на
VIII и
X
итоговых открытых научно-практических конференциях молодых ученых «Молодежь и
медицинская наука в
XXI
веке» (Киров, 2003, 2005); на ежегодных заседаниях научно-практического общества
терапевтов г.Кирова, на научно-практической конференции «Актуальные вопросы
трансфузиологии и клинической медицины» (Киров 2005).
ВНЕДРЕНИЕ В ПРАКТИКУ.
Результаты
работы внедрены в практику ревматологического отделения городской клинической
больницы №6 г. Кирова, материалы исследования используются в учебном процессе
Кировской государственной медицинской академии, докладываются практическим
врачам на научно-практических конференциях.
ОБЬЕМ И СТРУКТУРА
ДИССЕРТАЦИИ.
Диссертация изложена на 144 страницах, состоит из введения, обзора литературы, 3
глав собственных исследований, обсуждения, выводов, практических рекомендаций,
приложения. Диссертация иллюстрирована 19 таблицами, 17 рисунками, приведены 5
клинических примеров, указатель литературы содержит 236 источников, из них 84
отечественных и 152 зарубежных.
МАТЕРИАЛ И МЕТОДЫ
ИССЛЕДОВАНИЯ
Характеристика
клинического материала
Обследовано 93 больных достоверным АС,
соотношение мужчин и женщин составило 64:29, средний возраст 36,1 лет, средняя
длительность болезни 6,8 лет,
I
степень активности установлена у 9,
II
– у 58 и III
– у 26 больных. У 8 больных выявлена
I
- R-стадия
сакроилеита, у 37 – II,
у 41 – III
и у 7 больных – IV,
соотношение центральной и периферической форм 45:48. Из экстраартикулярных
проявлений встречались лихорадка (21), похудание (15), анемия (14), иридоциклит
(10), полинейропатия (3). Таким образом, у всех больных имелись признаки
активности заболевания. 33 больных на
разных сроках болезни получали до включения в исследование базисные препараты,
включая метотрексат (12) и сульфасалазин (21), которые были отменены в связи с
отсутствием эффекта или из-за тяжелых побочных действий за 9-10 недель до начала
лечения. У 23 больных с АС терапия проспидином была назначена в качестве первого
варианта базисной терапии.
Критерии включения
больных в исследование
Критериями включения пациентов в исследование
считали: достоверный диагноз АС (согласно Нью-Йоркским критериям, 1984), наличие
признаков активности заболевания, отсутствие эффекта от стабильной
противовоспалительной терапии в течение 3х-4х недель до начала терапии,
отсутствие тяжелой сопутствующей патологии внутренних органов с функциональной
недостаточностью, информированное согласие больного.
Критерии
исключения
Критериями исключения считали: АС без признаков
активности, на вторичный амилоидоз почек, сопутствующая патология внутренних
органов с функциональной недостаточностью, инфекционные заболевания,
организационные сложности контроля за проводимой терапией.
Методика
применения проспидина у больных АС
В работе использовался
проспидин Пермского научно-производственного объединения “Биомед” по 0,1г сухого
вещества в ампуле, который растворяли в 5мл физиологического раствора (для в/м
инъекций) или в 200мл 5% раствора глюкозы (для в/в вливаний). Проспидин
назначали после пробной дозы на индивидуальную переносимость в дозе 50 мг в/м.
В стационаре больные получали проспидин 200-300 мг/неделю в/в капельно на 200 мл
5% глюкозы N4.
Поддерживающую терапию проводили проспидином в дозе 100-200 мг/неделю в/м (в
зависимости от активности заболевания и эффективности терапии).
Пациенты методом
адаптивной рандомизации были разделены на три группы, сопоставимые по
клиническим и лабораторным показателям. Были сформированы три группы больных в
зависимости от вида проводимой терапии.
Первая группа (n=30)
получали только терапию НПВС (диклофенак натрия в дозе 150мг в сутки). Вторая
группа (n=33)
получали терапию проспидином в сочетании с теми же дозами НПВС. Третья группа (n=30) получали метотрексат (МТ) в сочетании с НПВС.
Метотрексат назначали в дозе 10 мг/нед. в/м.
Клинические и
инструментальные методы исследования
Для оценки эффективности
терапии использовали критерии оценки суставного синдрома. При этом определяли:
1) Суставной индекс (1-4 балла), 2) Общую оценку боли по ВАШ (0-100 мм). 3)
Длительность утренней скованности в минутах. 4) Количество воспаленных
(припухших) суставов. 5) Количество болезненных суставов. 6) Позвоночный индекс.
7) Индекс активности
BASDAI
8) Оценку функциональных возможностей пациентов (HAQ,
HAQ-S,
BASFI).
9) Оценка эффективности терапии по критериям
ASAS.
10) Оценка качества жизни пациентов проводилась при помощи общего опросника
SF
36. Кроме клинической оценки суставного синдрома использовали весь комплекс
лабораторного обследования больных, как для активного выявления
противопоказаний, так и для контроля за возможными побочными действиями. В этот
комплекс включались: общий анализ крови с подсчетом тромбоцитов, биохимические
исследования крови (СРБ иммунотурбометрическим методом (нормальный показатель до
10 мг/дл), фибриноген, мочевина, креатинин, билирубин, АЛТ, АСТ), анализы мочи.
Из инструментальных методов в процессе обследования использовались: ЭКГ, ЭхоКГ,
УЗИ суставов, стандартные рентгенограммы крестцово-подвздошных сочленений
(стадия по
Kellgren),
позвоночника для определения рентгенологической стадии заболевания, УЗИ органов
брюшной полости и почек для выявления экстраартикулярных проявлений и возможных
побочных действий препаратов.
Иммунологические методы
1) Определение концентрации сывороточных иммуноглобулинов: определение
содержания сывороточных иммуноглобулинов классов A,
M, G проводилось методом
радиальной иммунодиффузии по Mancini et.
al. В контрольной группе (n=56)
показатели принимали следующие значения: Ig A (1,87±0,18г/л),
Ig G (12,47±0,54
г/л), Ig M (1,05±0,06г/л).
2) Определение циркулирующих иммунных комплексов: циркулирующие иммунные
комплексы (ЦИК) в сыворотке крови определяли методом преципитации в растворе
полиэтиленгликоля (ПЭГ) по Haskown в модификации Ю.А.Григорович и А.Н.Алферовой.
В контрольной группе доноров (n=24) показатели ЦИК
52,8±4,5 ед.опт.пл.
3) HLA – типирование.
Определение стабильных метаболитов оксида азота
Стабильные метаболиты оксида азота определяли в сыворотке крови и моче методом
спектрофотометрии с реактивом Грисса до лечения и через 3, 6, 12 месяцев
терапии. В контрольной группе (n=35) показатели
содержания стабильных метаболитов оксида азота в сыворотке крови: 4,2 ± 0,78
мкг/л, в моче: 2,1 ± 0,45 мкг/л.
Статистическая обработка полученных результатов. По каждому
признаку определяли среднюю величину (М) и среднее квадратичное отклонение (s),
изучение динамики исследуемых показателей в процессе лечения проводили с помощью
парного t - критерия Стьюдента. Анализ качественных
признаков в сравниваемых группах – критерий
c2.
Во всех случаях нулевую гипотезу отвергали при p<0,05.
Анализ силы связи количественных признаков проводили, используя коэффициент
корреляции (r) Спирмена.
ПОЛУЧЕННЫЕ РЕЗУЛЬТАТЫ И ИХ ОБСУЖДЕНИЕ
Клинический анализ применения терапии проспидином
при анкилозирующем спондилоартрите
Лечение начинали в условиях специализированного ревматологического отделения,
после тщательного клинико-лабораторного обследования для уточнения диагноза и
выявления противопоказаний и получения письменного согласия больных на лечение.
В процессе применения терапии проспидином проводили изучение клинических,
лабораторных, инструментальных и некоторых иммунологических показателей болезни.
Оценку изучаемых параметров проводили до лечения, в конце стационарного этапа
лечения и в динамике через 3, 6, 12 месяцев терапии.
Клинический эффект проспидина у больных АС
проявлялся достаточно быстро уже на стационарном этапе (конец 2-ой начало 3-ей
недели лечения), что выражалось уменьшением боли и скованности в позвоночнике и
суставах, снижением суставного индекса и энтезопатий. Наибольшего изменения к 1
месяцу терапии претерпели такие показатели, как болевой синдром в позвоночнике и
суставах, выраженность и длительность утренней скованности, суставной индекс,
достоверно уменьшилось количество воспаленных суставов. Быстрота наступления
клинического эффекта на ранних этапах терапии, очевидно, связана с особенностями
механизма действия проспидина, обладающего наряду с иммунодепрессивным и
самостоятельным противовоспалительным действием. В процессе поддерживающей
терапии клинический эффект проспидина продолжал нарастать к 3-6 месяцу лечения
и сохранялся к 12 месяцу терапии по всем оцениваемым показателям. Индекс
активности BASDAI,
наиболее отражающий положительную динамику проводимой терапии АС, достоверно
снижался к 3 месяцу и далее на всех этапах наблюдения на фоне терапии
проспидином (рис.1). В группах больных, получавших НПВС и МТ, также было
отмечено улучшение оцениваемых показателей. Однако снижение этих показателей
происходило заметно медленней (через 4-5 недель терапии МТ и 8-10 недель терапии
НПВС) и было менее выражено по сравнению с терапией проспидином. На фоне терапии
НПВС и МТ улучшение сохранялось до 6 месяцев терапии, а к 12 месяцу по некоторым
показателям (выраженность скованности, боль в позвоночнике и суставах, число
болезненных суставов и суставной индекс) не выявлено нарастания положительного
клинического эффекта, а в ряде случаев отмечено ухудшение заболевания по этим
показателям.
Было изучено влияние терапии на показатели,
отражающие функциональные возможности пациентов в процессе лечения (рис.2, 3).
Под влиянием терапии проспидином наблюдалась положительная динамика показателей,
отражающих функциональный статус больных (HAQ,
HAQ-S,
BASFI).
При анализе показателей на фоне проводимой терапии
HAQ
достоверно снижались уже на стационарном этапе лечения, наиболее быстрая
положительная динамика шкалы
HAQ
наблюдалась, вероятно, за счет уменьшения боли и скованности в периферических
суставах. Функциональная способность пациентов, оцениваемая с помощью
HAQ-S
и BASFI,
отражающая в большей мере функциональные возможности позвоночника также
улучшалась к 1 месяцу терапии, с нарастанием положительного эффекта к 3-6
месяцу. Улучшение всех функциональных показателей сохранялось при дальнейшем
наблюдении (6, 12 месяцев), что достаточно хорошо отражает положительный эффект
от проводимой терапии и соответствует положительной динамике основных
клинических показателей снижения активности заболевания. Под влиянием терапии
НПВС и МТ, как и в группе больных, получавших проспидин, выявлена наиболее
быстрая динамика по шкале
HAQ, однако лишь к 3 месяцу терапии.
Показатели HAQ-S
и BASFI
в I
и III
группах наблюдения снижались медленнее по сравнению с
II.
В группах больных, получавших НПВС и МТ, значения
HAQ-S
были достоверны лишь на 6 месяце терапии. На фоне терапии МТ к 12 месяцу
наблюдения сохранялось улучшение показателей
HAQ
и BASFI,
на фоне НПВС отмечено ухудшение по всем показателям функционального статуса.
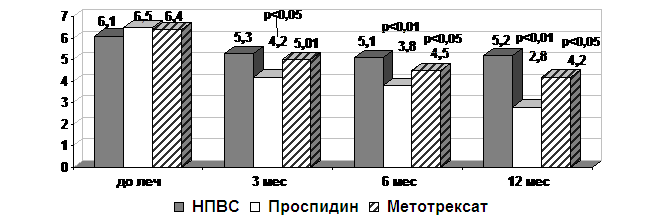
Рис.1. Динамика
BASDAI
под влиянием терапии
(р-достоверность различий
по отношению к показателям до лечения)
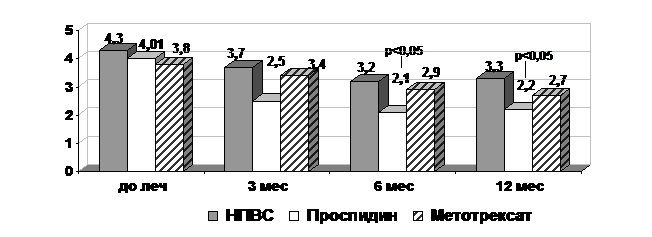
Рис. 2. Динамика
BASFI
в процессе терапии
(р-достоверность различий
по отношению к показателям до лечения)
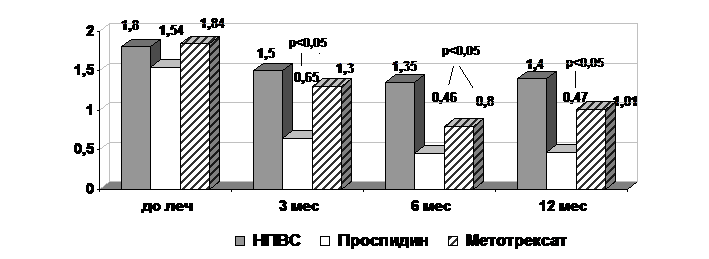
Рис. 3. Динамика
HAQ-S
в процессе терапии
(р-достоверность различий
по отношению к показателям до лечения)
У ряда больных (n=6)
оценка клинической эффективности проспидина была проведена и после 12 месяцев
терапии. У 3 больных наблюдалось сохранение улучшения до 18 месяцев, у 2 -
выявлено обострение заболевания с клиническими признаками активности процесса,
что потребовало коррекции терапии, у 1 больного - аллергическая реакция с
последующей отменой препарата.
При анализе
экстраартикулярных проявлений болезни (исходно всего 63) установлено, что чаще
других у больных АС регистрировались лихорадка, анемия и похудание во всех трех
группах наблюдения. При изучении сравнительного влияния терапии на
экстраартикулярные проявления болезни нами были получены следующие результаты,
представленные на рис. 4.
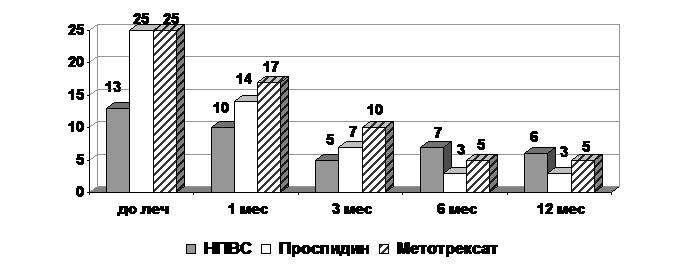
Рис. 4. Динамика
экстраартикулярных проявлений под влиянием терапии
Как видно из рис. 4,
положительная динамика более 50% экстраартикулярных проявлений наблюдалась к 3
месяцу терапии во всех группах. На фоне терапии проспидином (по сравнению с МТ)
она была больше выражена в отношении похудания и лихорадки. К 12 месяцу терапии
в группе больных, получавших НПВС экстраартикулярные проявления сохранялись в
количестве 6 (до лечения – 13), на фоне терапии проспидином произошло уменьшение
экстраартикулярных проявлений с 25 до 3, под влиянием терапии МТ с 25 до 5. На
основании того, что терапия проспидином и МТ (по сравнению с терапией НПВС) у
больных анкилозирующим спондилоартритом позволила купировать большинство
экстраартикулярных проявлений, можно косвенно судить о патогенетической
направленности и базисных свойствах данных препаратов.
При оценке общих
результатов лечения с использованием критериев
ASAS
выявлено, что значительное улучшение (ASAS
50% и 70%) отмечено к 3 месяцу лечения у 20 больных (64,5%), а к 12 месяцу
лечения у 19 больных (76%) на фоне терапии проспидином. В группах больных,
получавших НПВС и МТ, на всех этапах наблюдения было больше случаев с меньшим
клиническим эффектом, а показатели
ASAS70%
наблюдались лишь в единичных случаях (рис. 5).
Среди больных, у которых
была установлена частичная ремиссия на фоне терапии проспидином (ASAS70%),
у 3 пациентов стаж анкилозирующего спондилоартрита был менее 6 месяцев, у 2 –
менее 5 лет и у 2 пациентов стаж заболевания был 6-8 лет. Периферическую форму
анкилозирующего спондилоартрита в этой группе имели 5 больных и 2 пациента –
центральную. Среди больных с критериями улучшения 50% 8 пациентов имели
периферическую форму, 4 – центральную. В группе больных, получавших МТ,
улучшение 50 и 70% установлено у 8 пациентов, большинство из них (6 больных)
имели периферическую форму.
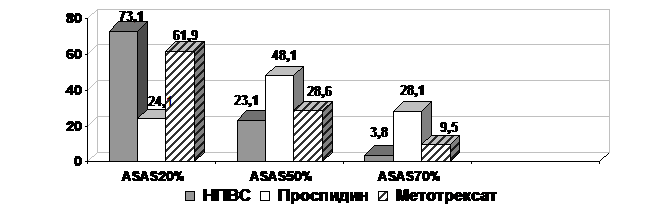
Рис. 5. Общая оценка
эффективности лечения (ASAS)
на фоне терапии НПВС, проспидином и метотрексатом (12 месяцев)
Анализируя полученные
данные, можно судить о некоторых закономерностях, которые по нашему мнению
оказывали влияние на развитие ремиссии заболевания. Более раннее и длительное
клиническое улучшение наблюдалось у больных со стажем АС менее 5 лет и с ранним
началом базисной терапии (особенно при наличии высокой активности заболевания).
Полученная нами положительная клиническая динамика на фоне терапии проспидином
наблюдалась у больных с периферической и центральной формами анкилозирующего
спондилоартрита, на фоне терапии МТ – преимущественно с периферической формой.
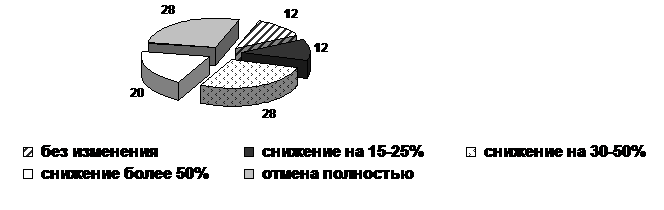 


Снижение дозы НПВС на фоне
проводимой терапии считается одним из важных показателей эффективности базисной
терапии. При изучении влияния терапии проспидином на суточную потребность в
НПВС у больных анкилозирующим спондилоартритом были получены следующие
результаты: под влиянием терапии проспидином удалось снизить суточную
потребность в НПВС без ущерба для общих результатов лечения, причем у 12%
больных - на 15-25% от исходной, у 28% больных – на 30-50% от исходной, у 20%
больных – на 50% и более, у 7 пациентов НПВС удалось отменить полностью (рис.
6).
Рис. 6. Влияние терапии
проспидином (I) и метотрексатом (II)
на суточную дозу НПВС (12
месяцев) (количество больных).
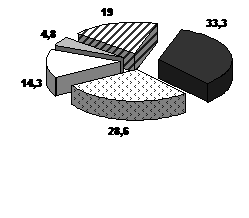
По сравнению с проспидином,
на фоне терапии МТ у 33,3% больных суточная доза НПВС снижена на 15-25% от
исходной, у 28,6 – на 30-50%, у 14,3 – на 50% и более и только у одного пациента
была возможна отмена НПВС полностью.
В таблице 1 представлена суточная потребность в НПВС под влиянием терапии
проспидином и МТ. Как видно из таблицы, более выраженный клинический эффект
проспидина (по сравнению с группой больных, получавших МТ) проявлялся и в
возможности существенно (почти на 30%) уменьшить суточную потребность в НПВС в
этой группе больных к 3 месяцу терапии, с сохранением положительного эффекта к
12 месяцу наблюдения. В группе больных, получавших МТ, достоверное снижение
суточной дозы НПВС наблюдалось к 3 месяцу терапии, но к 6-12 месяцу суточная
потребность в НПВС вновь возрастала.
Таблица 1
Потребность в НПВС (мг/сутки) под влиянием
терапии проспидином и
метотрексатом (М±s)
|
Сроки (мес) |
До леч |
1 мес |
3 мес |
6 мес |
12 мес |
|
Проспидин |
150 |
64,8±32,3* |
56,2±31,4** |
41,8±24,1** |
43,3±27,2** |
|
Метотрексат |
150 |
83,6±22,7 |
66,9±28,6* |
74,1±20,4* |
81,1±30,4 |
Примечание: *-p<0,05,
**-p<0,01.
Достоверность различий по отношению к показателям до лечения.
Соответственно положительной динамике клинических показателей в процессе лечения
нами установлена нормализация (или улучшение) лабораторных и некоторых
иммунологических показателей на фоне терапии проспидином: СОЭ, СРБ, уровня
фибриногена, ЦИК, Ig основных классов.
Рис. 7. Сравнительная частота 20%-го и более
снижения СОЭ
Для оценки влияния заболевания на качество жизни больных проводили сравнительную
оценку показателей качества жизни больных АС и показателей здоровых лиц при
помощи общего опросника SF – 36 с вычислением 8
основных показателей (рис. 10).
Как видно из рисунка 10,
все показатели качества жизни были достоверно значимо хуже у больных АС в
сравнении со здоровыми лицами (p<0,001).
У больных АС в наибольшей степени изменялись показатели физического здоровья.
Физическое функционирование было снижено на 71%, показатель ролевого физического
функционирования – на 80%, показатель боли на 53% в сравнении со здоровыми
лицами.
Среди показателей качества жизни, характеризующих психологический компонент
здоровья, в большей степени было снижено ролевое эмоциональное функционирование
– на 72%, социальное функционирование и жизнеспособность в меньшей степени
соответственно на 33% и 23% в сравнении с нормальными показателями,
психологическое здоровье на 10% хуже, чем у здоровых лиц. На основании
проведенного сравнительного анализа можно сделать вывод о том, что АС
значительно ухудшает параметры качества жизни больных в сравнении со здоровой
популяцией: страдает физическое и психологическое состояние больных, нарушается
их социальная адаптация. Под влиянием терапии проспидином произошло улучшение
параметров качества жизни больных АС (рис. 10), при этом наиболее
чувствительными к терапии были показатели физического здоровья, менее
чувствительными – показатели психического здоровья. При проведении
сравнительного анализа влияния терапии НПВС, проспидином и МТ на качество жизни
больных АС выявлено, что во всех группах наблюдения терапия оказывала
положительное влияние на оцениваемые параметры, при этом различные показатели
меняются в разные сроки.
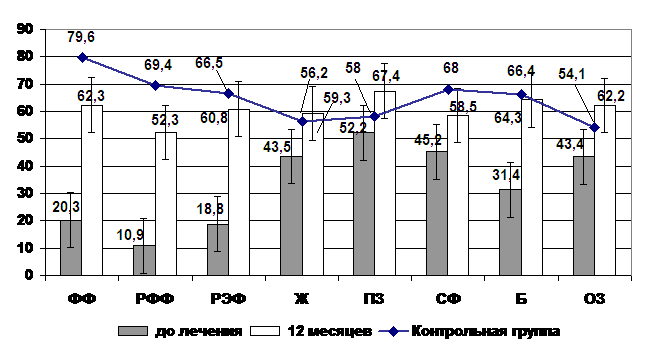
Рис. 10. Показатели качества жизни (опросник SF 36)
больных АС в процессе применения терапии проспидином и контрольной группы
Примечание: ФФ – физическое функционирование, РФФ – ролевое физическое
функционирование, РЭФ – ролевое эмоциональное функционирование, Ж –
жизнеспособность, ПЗ – психическое здоровье, СФ – социальное функционирование, Б
– боль, ОЗ – общее здоровье.
Проведено изучение уровней показателей
стабильных метаболитов оксида азота сыворотки крови и мочи у больных
анкилозирующим спондилоартритом (n=93) и группы здоровых доноров (n=35).
Концентрацию стабильных метаболитов оксида азота в сыворотке крови и моче
определяли с помощью реактива Грисса. Результаты исследования представлены в
таблице 2.
Как следует из таблицы 2, в группе больных
анкилозирующим спондилоартритом содержание стабильных метаболитов
NO
в сыворотке крови и моче было достоверно выше, чем в контрольной группе здоровых
доноров, и их концентрация повышалась с увеличением активности заболевания.
Содержание стабильных метаболитов оксида азота в сыворотке крови и моче больных
с III
степенью активности анкилозирующего спондилоартрита (сыворотка крови 27,9±4,6,
моча 17,3±3,2)
было достоверно выше (р<0,001), чем у больных с
II
степенью активности АС (сыворотка крови 22,2±4,6,
моча 15,5±3,2).
Таблица 2
Показатели содержания
стабильных метаболитов
NO в сыворотке крови и моче у больных АС и здоровых
лиц (М±s)
|
Стабильные метаболиты
NO
(мкг/л) |
Больные АС
(n=93) |
Здоровые доноры (n=35) |
р |
|
В крови |
24,5±8,7 |
4,2±0,78 |
< 0,05 |
|
В моче |
15,8±10,4 |
2,1±0,45 |
< 0,05 |
При проведении
корреляционного анализа уровня показателей стабильных метаболитов оксида азота и
некоторых клинических и лабораторных особенностей болезни отмечена прямая
умеренная корреляция уровня показателей стабильных метаболитов оксида азота
индексом активности
BASDAI,
длительностью утренней скованности, СРБ и фибриногеном. Содержание стабильных
метаболитов оксида азота в сыворотке крови имело обратную корреляцию с
длительностью заболевания, в группе больных со стажем болезни более 10 лет
выявлены наиболее низкие показатели стабильных метаболитов оксида азота.
Достоверных различий в зависимости от формы и стадии анкилозирующего
спондилоартрита не выявлено,
p>0,05
(таблица 3).
Таблица 3
Связь показателей стабильных метаболитов оксида азота
сыворотки крови и мочи с некоторыми
клинико-лабораторными особенностями болезни
|
Показатель |
Коэффициент корреляции |
Достоверность |
|
BASDAI |
0,396 |
Р<0,05 |
|
Длительность утренней скованности |
0,489 |
Р<0,01 |
|
СРБ |
0,31 |
Р<0,01 |
|
Фибриноген |
0,304 |
Р<0,05 |
|
Форма АС |
0,14 |
Р>0,05 |
|
R-стадия
сакроилеита |
0,21 |
Р>0,05 |
|
Стаж болезни |
-0,375 |
Р<0,05 |
При изучении динамики
показателей стабильных метаболитов оксида азота в процессе терапии НПВС,
проспидином и МТ были получены следующие результаты (рис. 11).
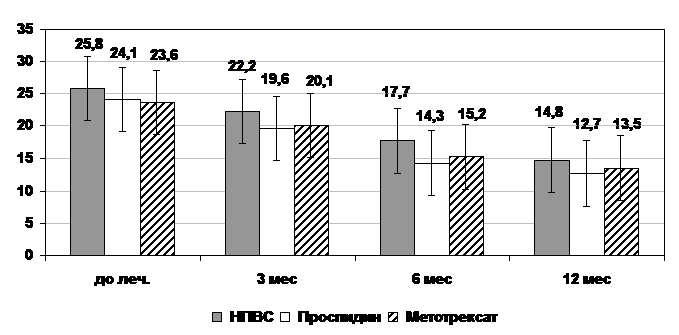
Рис. 11. Содержание стNO
(мкг/л) в сыворотке крови у больных АС в процессе терапии
Как видно из рис. 11 к 3
месяцу лечения во всех группах наблюдалась тенденция к снижению уровня
стабильных метаболитов оксида азота по сравнению с показателями до лечения. К 6
месяцу терапии в группе больных, получавших проспидин, отмечено достоверное
снижение показателей стабильных метаболитов оксида азота в сыворотке крови и
моче (p<0,05),
на фоне терапии МТ – в сыворотке крови (p<0,05). К 12 месяцам терапии уровень стабильных
метаболитов оксида азота сыворотки крови снижался, а в моче несколько возрастал,
но продолжал оставаться ниже, чем до начала лечения
Таким образом, определение
стабильных метаболитов оксида азота в сыворотке крови и моче имеет определенное
клиническое значение. Повышение их уровня у больных анкилозирующим
спондилоартритом по сравнению с группой здоровых доноров и с нарастанием
активности процесса указывает на их диагностическое значение в качестве
лабораторного показателя активности. Отмеченная динамика концентрации стабильных
метаболитов оксида азота под влиянием терапии говорит о прогностической ценности
данного показателя.
Переносимость терапии проспидином в проведенном исследовании была вполне
удовлетворительной. В отдельных случаях в момент введения пробной дозы
проспидина (50мг) в/м препарата возникало легкое головокружение, чувство жара,
«приливы» к лицу. Эти явления были кратковременными (от 15-20 минут до 1-2
часов), больше выражены при внутривенном способе введения и уменьшались или
совсем отсутствовали в случае горизонтального положения больных в момент
введения и были минимальными при внутримышечном способе введения проспидина на
амбулаторном этапе.
При сравнении переносимости проспидина, МТ и НПВС (таблица 4) в процессе терапии
у больных анкилозирующим спондилоартритом выявлено, что переносимость препаратов
была вполне удовлетворительной. Побочные действия в группе больных, получавших
проспидин, зарегистрированы в 36,3% случаев (12 больных), они были нетяжелыми,
проявлялись преимущественно в парестезиях, диспептических явлениях (тошнота) и
потребовали отмены препарата у 7 больных (21,2%), главным образом на 6-9 месяце
терапии. Побочные действия МТ у 13 больных анкилозирующим спондилоартритом
(43,3%) в нашем исследовании в общем соответствовали его профилю токсичности.
Преобладали диспептические расстройства (тошнота, рвота), церебральные
расстройства (головокружения, слабость), повышение печеночных трансаминаз (более
чем в 3 раза). Частота отмен в этой группе больных была выше по сравнению с
группой получавших проспидин и составила 26,7% (8 больных) В группе больных,
получавших НПВС, побочные действия зарегистрированы у 11 больных (36,6%). Они
проявлялись характерными для данной группы препаратов токсическими реакциями.
Таблица 4
Сравнительный анализ
побочных действий и частота отмены в
процессе терапии НПВС,
проспидином и метотрексатом у больных АС
Побочные
действия
|
НПВС
|
Проспидин
|
Метотрексат
|
|
абс. |
% |
абс. |
% |
абс. |
% |
|
Парестезии |
|
|
3 (2) |
9,1 (6,1) |
|
|
|
Диспептические явления |
4 |
13,3 |
5 (3) |
15,1(9,1) |
5(3) |
16,7 (10) |
|
Гастропатии |
4 (2) |
13,3(6,7) |
|
|
|
|
|
Повышение трансаминаз |
2 |
6,7 |
|
|
3(2) |
10 (6,7) |
|
Головокружения,слабость |
|
|
2 (1) |
6,1 (3) |
3(2) |
10 (6,7) |
|
Аллергический дерматит |
|
|
2 (1) |
6,1 (3) |
1(1) |
3,3 (3,3) |
|
Преходящая протеинурия (0,04-0,3 г/л) |
|
|
|
|
1(0) |
3,3 (0) |
|
Повышение уровня АД |
1 |
3,3 |
|
|
|
|
|
Всего
|
11
(2) |
36,3
(6,7) |
12
(7) |
36,3
(21,2) |
13
(8) |
43,3
(26,7) |
Примечание: в скобках указана частота отмены
препаратов.
В процессе применения проспидина не отмечено
достоверно значимых изменений со стороны периферической крови и основных
лабораторных биохимических показателей, отражающих функциональное состояние
печени и почек, что указывает на отсутствие явного токсического влияния терапии
проспидином на данные показатели.
Таким образом, на основании проведенного анализа клинико-лабораторной и
иммунологической эффективности терапии проспидином при анкилозирующем
спондилоартрите, сравнении ее с другими видами базисной терапии, а также
симптоматической терапией НПВС, установлено, что терапия проспидином оказывает
достаточно быстрый (на 2-3 неделе лечения) и выраженный клинический эффект у
больных АС, по критериям ASAS 50 и 70% к 12 месяцу
терапии улучшение наступало у подавляющего числа больных. Наряду с клиническим
эффектом, на фоне терапии проспидином у больных происходит улучшение ряда
лабораторных и иммунологических показателей, отражающих активность заболевания.
Применение терапии проспидином позволяет уменьшить суточную потребность в НПВС.
Побочные действия терапии проспидином в большинстве случаев являются нетяжелыми,
обратимыми и требуют отмены препарата в 21,2% случаев. При сравнении
эффективности предложенного нами способа лечения больных АС с результатами
клинической эффективности метотрексата и НПВС, можно говорить о преимуществе
терапии проспидином. Установленная высокая эффективность и вполне
удовлетворительная переносимость предлагаемого метода позволяет рекомендовать
его для лечения центральной и периферической форм АС, с экстраартикулярными
проявлениями.
ВЫВОДЫ
1.
Терапия проспидином у больных анкилозирующим спондилоартритом оказывает
быстрый (на 4 неделе лечения) и выраженный клинический эффект по
непосредственным и отдаленным (12 месяцев) результатам лечения. По критериям
ASAS
50 и 70% к 12 месяцу терапии улучшение наступало у 76% больных. Применение
терапии проспидином позволяет уменьшить суточную потребность в НПВС в процессе
лечения.
2.
Терапия проспидином улучшает функциональные показатели у больных
анкилозирующим спондилоартритом и оказывает положительное влияние на показатели,
отражающие качество жизни больных.
3.
Влияние терапии проспидином на лабораторные и иммунологические показатели
проявляется в достоверном снижении и/или нормализации СОЭ (к 12 месяцам
уменьшение на 20% и более у 80% больных), концентрации СРБ (20%-е уменьшение у
84,1% больных), иммуноглобулинов основных классов и ЦИК (20%-е снижение у 88,1%
больных). Выраженность иммунодепрессивного воздействия соответствовала
клиническим результатам лечения.
4.
Побочные действия, возникающие в процессе применения терапии проспидином,
встречаются в 36,3% случаев. Побочные действия являются в основном
доброкачественными, проходят самостоятельно и не требуют дополнительной
коррекции. Максимальное количество отмен препарата в связи с побочными эффектами
выявлено на 6-9 месяце лечения. Проспидин не оказывает угнетающего действия на
систему кроветворения и токсичного влияния на печень и почки.
5.
При сравнительном исследовании терапии проспидином, НПВС и метотрексатом
установлено, что проспидин по эффективности, срокам наступления клинического
эффекта и его выраженности превосходит НПВС и метотрексат у больных
анкилозирующим спондилоартритом.
6.
Установлено повышение концентрации стабильных метаболитов оксида азота у
больных АС, повышение их концентрации зависит от активности заболевания. Терапия
оказывает нормализующее влияние на показатели стабильных метаболитов оксида
азота сыворотки крови и мочи у больных АС в процессе лечения, что может
рассматриваться как дополнительный лабораторный критерий эффективности
проводимой терапии при АС.
7.
Высокая клиническая эффективность терапии проспидином, ее достаточно хорошая
переносимость позволяют рассматривать проспидин в качестве базисного средства в
терапии АС. Показанием к его назначению являются центральные и периферические
формы заболевания, экстраартикулярные проявления АС.
ПРАКТИЧЕСКИЕ РЕКОМЕНДАЦИИ
1.
Показаниями к применению терапии проспидином являются достоверный диагноз АС,
II-III степени активности, с
экстраартикулярными проявлениями.
2.
Терапию проспидином рекомендуется начинать в условиях стационара после
предварительного дообследования и определения индивидуальной чувствительности к
проспидину путем введения пробной дозы 50 мг проспидина растворенного 2,5 мл
физиологического раствора внутримышечно.
3.
Режим дозирования в стационаре. При хорошей переносимости проспидина, его
назначают в дозе 200-300 мг/сутки внутривенно капельно медленно на 200,0 мл 5%
раствора глюкозы 1 раз в неделю. Выбор дозы проспидина зависит от активности
болезни, переносимости препарата (при II степени
активности назначается 200 мг/сутки 1 раз в неделю, при III
степени активности назначается 300 мг/сутки 1 раз в неделю). Всего на
стационарном этапе проводят 4-5 введений проспидина.
4.
Поддерживающая терапия. Методика поддерживающей терапии выбирается индивидуально
и зависит от результатов стационарного этапа лечения. На
амбулаторно-поликлиническом этапе рекомендуется вводить проспидин в дозе 100-200
мг внутримышечно 1 раз в неделю. При появлении признаков нарастания активности
дозу проспидина увеличивают до 200-300 мг в неделю. В дальнейшем при условии
хорошего эффекта от проводимой терапии и минимальной активности болезни
проспидин рекомендуется делать в той же дозе, увеличивая интервал до 2 недель.
5.
Лабораторными показателями для назначения терапии проспидином и контролем за ее
эффективностью могут служить концентрации СРБ, уровень иммуноглобулинов основных
классов и ЦИК, из дополнительных методов – повышения уровня стабильных
метаболитов оксида азота сыворотки крови и мочи. Лабораторными методами контроля
за возможными побочными действиями терапии проспидином являются: общий анализ
крови с тромбоцитами, определение уровня билирубина и печеночных ферментов АлТ,
АсТ, определение уровня мочевины, креатинина сыворотки крови, общий анализ мочи.
6.
В
процессе терапии необходимо контролировать побочные действия терапии проспидином,
которые проявляются в основном парестезиями, повышенной чувствительностью к
холоду, головокружениями, головной болью, диспептическими явлениями. Эти
побочные действия носят, как правило, преходящий характер и проходят
самостоятельно при уменьшении дозы препарата. Появление аллергического дерматита
и тяжелых церебральных расстройств, требует отмены препаратов. Во время
внутривенного введения проспидина возможно появление чувства жара, легкого
головокружения, приливов к лицу. Эти ощущения кратковременны, проходят
самостоятельно и легче переносятся больными при введении препарата в положении
лежа.
7.
Противопоказаниями к назначению терапии проспидином являются: индивидуальная
непереносимость препарата, нарушение функции почек, печени, тяжелые
сопутствующие заболевания внутренних органов с функциональной недостаточностью,
сахарный диабет, цереброваскулярная недостаточность, инфекционные заболевания.
Список работ, опубликованных по теме
диссертации.
1.
Клинические особенности серонегативных спондилоартритов. Актуальные
проблемы современной ревматологии: Сборник научных работ. Волгоград; 2002.
113-114. соавт. Симонова О.В., Немцов Б.Ф.
2.
Взаимосвязь функционального состояния и показателей позвоночного индекса
у больных с серонегативными спондилоартропатиями. Материалы
VIII
итоговой открытой научно-практической конференции молодых ученых и студентов
«Молодежь и медицинская наука в
XXI
веке». Киров; 2003. 14-15.
3.
Клиническое значение показателей
стабильных метаболитов оксида азота у больных анкилозирующим спондилоартритом.
Актуальные проблемы современной ревматологии: Сборник научных работ. Волгоград;
2004. 117-118.
4.
Clinical efficacy of prospidin therapy in patients with ankylosing
spondylitis. Annual European Congress of Rheumatology “EULAR 2004”. Berlin,
Germany; 9-12 June 2004. SAT0006. соавт. B.F.Nemtsov, O.V.Simonova.
5.
Сравнительный анализ побочных действий базисной терапии у больных
анкилозирующим спондилоартритом. Научные труды
V
Международной научно-практической конференции «Здоровье и образование в
XXI
веке». Москва; 2004. 360. соавт. Немцов Б.Ф., Симонова О.В.
6.
Сравнительная оценка эффективности базисной терапии анкилозирующего
спондилоартрита. Научные труды
V
Международной научно-практической конференции «Здоровье и образование в
XXI
веке». Москва; 2004. 269. соавт. Немцов Б.Ф., Симонова О.В.
7.
Оценка качества жизни больных анкилозирующим спондилоартритом. Тезисы
научно-практической конференции «Социальные аспекты ревматических заболеваний».
Звенигород; 27-28 мая 2004. Научно-практическая ревматология. 2004; 2: 77. соавт.
Немцов Б.Ф., Симонова О.В.
8.
Влияние различных видов базисной терапии на функциональный статус больных
анкилозирующим спондилоартритом. Тезисы
IV
съезда ревматологов. Казань; 23-26 мая 2005. Научно-практическая ревматология.
2005; 2: 70. соавт. Немцов Б.Ф.
9.
Клиническая эффективность базисной терапии анкилозирующего
спондилоартрита и влияние на качество жизни. Актуальные проблемы современной
ревматологии: Сборник научных работ. Волгоград; 2005; выпуск
XXII:
141. соавт. Немцов Б.Ф.
10.
Применение нового базисного средства проспидин в терапии анкилозирующего
спондилоартрита. Тезисы научно-практической конференции «Актуальные вопросы
трансфузиологии и клинической медицины». Киров; 2005. 78. соавт. Немцов Б.Ф.
Список условных сокращений
АС - анкилозирующий спондилоартрит
ВАШ – визуальная аналоговая шкала
ГКС – глюкокортикостероиды
МТ - метотрексат
НПВС – нестероидные противовоспалительные
средства
П – проспидин
СОЭ – скорость оседания эритроцитов
СРБ – С-реактивный белок
ФНО-а – фактор некроза опухолей альфа
ЦИК – циркулирующие иммунные комплексы
NO
– оксид азота
стNO
– стабильные метаболиты оксида азота
|
