Р Е В М А Т О Л О Г И Я
Симонова
Ольга Викторовна
КОМБИНИРОВАННАЯ ТЕРАПИЯ
ПРОСПИДИНОМ И МЕТОТРЕКСАТОМ
ПРИ ХРОНИЧЕСКИХ ЭРОЗИВНЫХ
ЗАБОЛЕВАНИЯХ СУСТАВОВ
14.00.39
– ревматология
АВТОРЕФЕРАТ
диссертации на соискание ученой степени
доктора медицинских наук
Ярославль –
2004
Работа
выполнена в государственном образовательном учреждении высшего профессионального
образования «Кировской государственной медицинской академии Федерального
агенства по здравоохранению и социальному развитию Российской Федерации»
Научный консультант
|
доктор медицинских наук,
профессор Немцов Борис Федорович |
|
Официальные оппоненты: |
доктор медицинских наук, профессор
Коршунов Николай Иванович
доктор медицинских наук,
Ананьева Лидия Петровна
доктор медицинских наук,
Бадокин Владимир Васильевич |
|
|
|
Ведущая организация
Волгоградский государственный
медицинский университет
Защита состоится « 26 » октября 2004 г.
в ____ часов на заседании диссертационного совета Д 208.119.01 при
Ярославской государственной медицинской академии (150000, г. Ярославль, ул.
Революционная 5)
С диссертацией можно ознакомиться в
библиотеке Ярославской государственной медицинской академии
Автореферат разослан
« » 2004г.
Ученый секретарь
Диссертационного
Совета Зотов А.А.
Актуальность проблемы.
Хронические эрозивные заболевания суставов
включают в себя большое число нозологических форм, характеризующихся поражением
суставов и/или позвоночника воспалительного характера с развитием деструктивных
изменений и анкилозирования, что в свою очередь приводит к стойкой
функциональной недостаточности опорно-двигательного аппарата, а нередко и к
инвалидизации больных. Ревматоидный артрит (РА) и псориатический артрит (ПсА) –
основные представители хронических прогрессирующих эрозивных заболеваний
суставов иммуновоспалительной природы являются одной из главных проблем
ревматологии (В.А. Насонова, 1999; Е.Л. Насонов, 2003;
P.J.
Mease,
2002; M.E.
Weinblatt,
2003). Частота РА и ПсА в популяции достигает 1%, а распространенность ПсА
среди больных псориазом –13,5-47% (В.В. Бадокин, 2001; Р.М. Балабанова, 1997;
Е.Л. Насонов, 2003).
Фактически у двух третей больных РА
характеризуется медленным, но неуклонным прогрессированием с неполными
ремиссиями и частыми обострениями, приводящим к ранней потере трудоспособности
(примерно в половине случаев в первые 6 лет болезни). Нередко с самого начала
ПсА протекает с выраженным экссудативным компонентом в пораженных суставах,
максимальной активностью воспалительного процесса, характеризуется быстро
прогрессирующим течением с развитием стойкой функциональной недостаточности
опорно-двигательного аппарата уже в течение первых двух лет болезни (В.В.
Бадокин, 2002; N.J.
McHugh,
2003). Все это позволяет рассматривать РА и ПсА как одни из самых тяжелых
хронических заболеваний человека.
В последние годы в лечении РА и ПсА достигнуты
существенные успехи, связанные с углубленным изучением патогенеза, разработкой и
внедрением в практику новых методов лечения. Тем не менее, неудовлетворенность
результатами терапии, особенно при длительном наблюдении требует постоянного
поиска новых и совершенствования существующих методов лечения, способных не
только подавлять активность, но и модифицировать течение болезни (Е.Л. Насонов,
Н.В. Чичасова, 1999; Я.А. Сигидин, Г.В. Лукина, 2001; Е.Л. Насонов, 2002;
P.J.
Mease,
2002; M.E.
Weinblatt,
2003). Один из способов повышения эффективности терапии РА и ПсА – применение
комбинации нескольких базисных препаратов. В настоящее время не сложилось
однозначного мнения о безусловной эффективности комбинированной терапии при РА и
ПсА. Некоторые из комбинаций, вопреки ожиданиям, не оказывали лечебного
воздействия (E.F.
Morand,
1999; R.F.
Wilkens,
1992). В то же время в ряде работ результаты комбинированной базисной терапии
оказались весьма эффективными (Я.А. Сигидин, Ю.В. Муравьев, Г.Н. Жуковская,
1990; M.
Gonzaiez-Gay,
1998; J.M.
Kremer,
1998; P.E.
Lipsky,
2000; G.
Provenzano,
2003). Таким образом, проблема эффективности комбинированной терапии РА и ПсА
требует дальнейшего изучения.
Учитывая то, что метотрексат считается «золотым
стандартом» фармакотерапии РА и ПсА (В.В. Бадокин, 2003; Е.Л. Насонов, 2002;
G.S.
Alarcon,
1997), а проспидин, как установлено нами ранее, достаточно высоко эффективен в
качестве монотерапии при лечении РА (Е.В. Бененсон, Б.Ф. Немцов, О.В. Симонова,
1994) нами была предложена новая комбинация двух базисных препаратов для лечения
РА и ПсА – проспидина и метотрексата. При создании этой комбинации мы исходили
из основных принципов комбинированной терапии: каждый из препаратов обладает
самостоятельным клиническим эффектом, препараты имеют разные механизмы действия
и различный спектр побочных действий. В литературе мы не обнаружили данных о
комбинированном применении проспидина и метотрексата в ревматологии, в том числе
при РА и ПсА. В связи с этим нам представляется перспективным изучение
клинической эффективности комбинированной терапии проспидином и метотрексатом
при РА и ПсА, включая открытое, контролируемое исследование и сравнительный
анализ с монотерапией метотрексатом и проспидином. Эти предпосылки и послужили
теоретическим обоснованием к проведению наших исследований.
Цель работы:
обоснование применения комбинированной терапии проспидином и метотрексатом при
РА и ПсА и доказательство ее клинической эффективности в открытом сравнительном
контролируемом исследовании.
Задачи работы:
1.
Провести сравнительный анализ клинической эффективности комбинированной
терапии проспидином и метотрексатом и монотерапии проспидином при РА.
2.
Провести сравнительный анализ клинической эффективности комбинированной
терапии проспидином и метотрексатом и монотерапии метотрексатом при РА по их
влиянию на клинические проявления болезни, суточную потребность в нестероидных
противовоспалительных препаратах и стероидах, возможность индукции и удержания
ремиссии в процессе длительного лечения (срок наблюдения 36 месяцев), частоту
и характер побочных действий.
3.
Оценить влияние комбинированной терапии проспидином и метотрексатом в
сравнении с монотерапией метотрексатом на темпы рентгенологического
прогрессирования, функциональный статус и качество жизни больных РА по
непосредственным и отдаленным (36 месяцев) результатам лечения.
4.
Оценить клиническую эффективность комбинированной терапии проспидином и
метотрексатом у больных ранним РА.
5.
Провести сравнительный анализ клинической эффективности комбинированной
терапии проспидином и метотрексатом и монотерапии метотрексатом у больных ранним
РА.
6.
Провести сравнительный анализ клинической эффективности комбинированной
терапии проспидином и метотрексатом и монотерапии метотрексатом при ПсА по их
влиянию на клинические проявления болезни, возможность индукции и удержания
ремиссии в процессе лечения, суточную потребность в нестероидных
противовоспалительных препаратах, частоту и характер побочных действий.
7.
Оценить влияние комбинированной терапии проспидином и метотрексатом в
сравнении с монотерапией метотрексатом на темпы рентгенологического
прогрессирования, функциональный статус и качество жизни больных ПсА.
8.
Разработать рациональную методику применения комбинированной терапии
проспидином и метотрексатом при РА и ПсА.
Научная новизна:
Впервые проведен сравнительный анализ
клинической эффективности комбинированной терапии проспидином и метотрексатом с
монотерапией проспидином в открытом контролируемом исследовании при РА.
Впервые проведен сравнительный анализ
клинической эффективности комбинированной терапии проспидином и метотрексатом с
монотерапией метотрексатом в открытом контролируемом исследовании при РА.
Впервые изучена клиническая эффективность
комбинированной терапии проспидином и метотрексатом у больных ранним РА.
Впервые проведен сравнительный анализ
клинической эффективности комбинированной терапии проспидином и метотрексатом и
монотерапии метотрексатом у больных ранним РА.
Впервые изучена клиническая эффективность
комбинированной терапии проспидином и метотрексатом при ПсА, ее влияние на
суточную потребность в нестероидных противовоспалительных препаратах,
возможность вызывать ремиссию.
Впервые изучена переносимость, частота и
характер побочных действий комбинированной терапии проспидином и метотрексатом
у больных ПсА.
Впервые изучено влияние комбинированной терапии
проспидином и метотрексатом на темпы рентгенологического прогрессирования,
функциональный статус и качество жизни больных ПсА.
Впервые проведен сравнительный анализ
клинической эффективности комбинированной терапии проспидином и метотрексатом с
монотерапией метотрексатом при ПсА в открытом контролируемом исследовании по
их влиянию на клинические проявления болезни, возможность индукции и удержания
ремиссии в процессе лечения, суточную потребность в нестероидных
противовоспалительных препаратах, частоту и характер побочных действий, темпы
рентгенологического прогрессирования, функциональный статус и качество жизни.
Научная новизна работы подтверждена: 1) патентом
на изобретение «Способ лечения ревматоидного артрита», №2199320 от 27.02.2003 г.
Авторы Б.Ф.Немцов, О.В.Симонова, Е.В.Бененсон, Н.Н.Политова; 2) патентом на
изобретение «Способ лечения псориатического артрита», №.2228755 от 20.05.2004 г.
Авторы Б.Ф. Немцов, О.В. Симонова.
Практическое значение работы:
Разработана рациональная методика применения
комбинированной терапии проспидином и метотрексатом при РА и ПсА, включающая:
1) дозы, интервал введения препаратов на
стационарном этапе и в процессе наблюдения до 36 месяцев;
2) показания и противопоказания к ее применению;
3) критерии для назначения лечения, контроля за
ее эффективностью и выявления возможных побочных действий.
Установлено раннее наступление клинического
эффекта при применении комбинированной терапии, сохраняющееся в сроки до 36
месяцев.
Установлена клиническая эффективность
комбинированной терапии проспидином и метотрексатом у больных ранним РА.
Выявлены основные побочные эффекты
комбинированной терапии проспидином и метотрексатом и показана их
доброкачественность и обратимость при РА и ПсА.
Комбинированная терапия проспидином и
метотрексатом способствует расширению возможностей базисной терапии
неблагоприятных вариантов РА и ПсА, включая резистентные к другим видам
проводимой базисной терапии.
Основные положения, выносимые на защиту:
1.
Комбинированная терапия проспидином и метотрексатом обладает более выраженным
клиническим эффектом при РА, по сравнению с монотерапией проспидином, при
оценке ближайших и отдаленных результатов лечения.
2.
Комбинированная терапия проспидином и метотрексатом, по сравнению с монотерапией
метотрексатом, обладает быстро наступающим и более выраженным клиническим
эффектом при РА при оценке на стационарном этапе, ближайших и отдаленных
результатов лечения, в том числе при раннем РА.
3.
Комбинированная терапия проспидином и метотрексатом обладает выраженным
клиническим эффектом у больных ПсА, позволяет подавлять активность болезни уже
на ранних этапах лечения, замедляет темпы рентгенологического
прогрессирования, улучшает функциональный статус и качество жизни.
4.
Комбинированная терапия проспидином и метотрексатом, по сравнению с монотерапией
метотрексатом, обладает быстро наступающим и более выраженным клиническим
эффектом при ПсА при оценке на стационарном этапе, ближайших и отдаленных
результатов лечения.
5. Применение
комбинированной терапии проспидином и метотрексатом расширяет возможности
базисной терапии тяжелых вариантов РА и ПсА, резистентных к другим видам
проводимой базисной терапии.
Публикации. По
теме диссертации опубликовано 45 научных работ, из них 32 в центральной
печати, 10 в зарубежной печати.
Апробация работы.
Основные положения диссертации доложены на III
съезде ревматологов, г. Рязань 2001 г.; VII итоговой
открытой научно-практической конференции молодых ученых «Молодежь и медицинская
наука в XXI веке», г. Киров 2001 г., 2002 г.; научной
сессии Вятского регионального отделения РАЕН, г. Киров 2001 г.; конференции
молодых ученых России, г. Звенигород 2002г.; Всероссийском конгрессе
ревматологов, Саратов 2003.; на заседаниях научно-практического общества
терапевтов г. Кирова.
Внедрение в
практику. Результаты работы внедрены в практику городского
ревматологического отделения городской клинической больницы №6 г. Кирова,
материалы исследования используются в учебном процессе Кировской государственной
медицинской академии. Практическая значимость подтверждена патентом на
изобретение «Способ лечения ревматоидного артрита», №2199320 от 27.02.2003 г. и
патентом на изобретение «Способ лечения псориатического артрита», №2228755 от
20.05.2004 г.
Объем и структура
диссертации: Диссертация изложена на 305 страницах, состоит из введения,
обзора литературы, 5 глав собственных исследований, обсуждения, выводов,
практических рекомендаций. Диссертация иллюстрирована 73 таблицами, 23
рисунками, приведены 16 клинических примеров, указатель литературы содержит 436
источников отечественных и зарубежных авторов.
МАТЕРИАЛ И МЕТОДЫ ИССЛЕДОВАНИЯ
Характеристика клинического материала
Исследование проведено у 276 больных
достоверным РА и больных достоверным ПсА. Среди больных РА (213) преобладали
женщины (188), средний возраст 47,1±7,3 года, средняя длительность болезни 5,4
лет, с полиартритическим суставным синдромом (213) и экстраартикулярными
проявлениями (170). 188 были серопозитивны по РФ, 59 больных нуждались в
постоянном приеме глюкокортикостероидов.
II
степень активности была установлена у 55 больных,
III
– у 158. У 23 больных выявлена
I
рентгенологическая стадия болезни, у 138 –
II,
у 52 – III.
Среди больных ПсА (63), включенных в исследование, преобладали женщины (42),
средний возраст 41,8±8,9 лет, средняя длительность суставного синдрома 4,7±5,2
лет, средняя длительность кожного псориаза 12,0±11,6 лет. Все больные ПсА имели
вульгарный очаговый (33) или распространенный (30) псориаз в прогрессирующей
(29) или стационарной (34) стадии, полиартритический вариант суставного синдрома
(63), II
(36) и III
(27) степень активности болезни. У 5 больных была установлена
I
рентгенологическая стадия болезни, у 35 –
II,
у 23 – III.
Около трети больных ПсА (23) имели системные проявления и тяжелую форму
заболевания. Большинство больных РА и ПсА получали до включения в исследование
различные виды терапии, включая базисные препараты, которые были отменены в
связи с отсутствием эффекта или из-за тяжелых побочных действий.
Критерии включения больных в исследование:
достоверный диагноз РА (соответствие критериям
АРА 1987 года) или ПсА (соответствие критериям Э.Р. Агабабовой и соавт. 1989
года), II-III
степень активности, наличие системных проявлений,
I-III
рентгенологические стадии болезни, отсутствие эффекта от нестероидных
противовоспалительных средств (НПВС) и предшествующей базисной терапии или ее
непереносимость, стероидозависимость, отсутствие приема базисных средств в
течение 6-8 недель до начала лечения, информированное согласие больного на
проведение терапии.
Критерии исключения:
РА или ПсА без признаков активности или
I
степени активности, IV
рентгенологическая стадия болезни, подозрение на вторичный амилоидоз почек,
беременность, лактация, сопутствующая патология внутренних органов с
функциональной недостаточностью, инфекционные заболевания, сахарный диабет,
организационные сложности контроля за лечением.
Методика применения комбинированной терапии и дозы препаратов:
Комбинированную терапию
проспидином и метотрексатом применяли у 75 больных достоверным РА и у 30 больных
достоверным ПсА. В работе использовался проспидин производства Пермского
научно-производственного объединения «Биомед» по 0,1 г сухого вещества в ампуле,
который растворяли в 2,5 мл физиологического раствора (для внутримышечных
инъекций) или в 200 мл 5% растворе глюкозы (для внутривенных вливаний). Препарат
назначали после предварительного определения индивидуальной чувствительности в
дозе 50 мг внутримышечно на 2,5 мл физиологического раствора. На стационарном
этапе больные получали проспидин 200-300 мг/нед. внутривенно капельно медленно
на 200 мл. 5% глюкозы. Всего в стационаре пациенты получали 4 -5 инъекций
проспидина. Метотрексат на стационарном этапе назначали в дозе 10мг/нед.
внутримышечно на 3-и сутки после введения проспидина. Лечение проводилось на
фоне приема НПВС и глюкокортикостероидов (ГКС) в дозах, которые больные
принимали до начала терапии в течение 2-3 недель без клинического эффекта. В
период лечения больным не проводились физиопроцедуры и локальная терапия ГКС.
Поддерживающую терапию на амбулаторном этапе проводили проспидином в дозе
100-200 мг/нед. внутримышечно, доза метотрексата оставалась прежней – 10 мг/нед.
При отсутствии эффекта в течение 6-8 недель, дозу проспидина увеличивали до
200-300 мг/нед. Причинами отмены комбинированной терапии проспидином и
метотрексатом считали индивидуальную непереносимость препаратов, тяжелые
побочные реакции, отсутствие клинического эффекта в течение 3 месяцев. В этом
случае терапию отменяли и назначали ГКС системно.
Клинические и
инструментальные методы исследования
Основу обследования больных составили
общеклинические методы, принятые в ревматологической клинике. При этом
определяли: суставной индекс (0-3 балла), общую оценку боли по ВАШ (0-100 мм),
длительность утренней скованности в минутах, количество воспаленных (припухших)
суставов, количество болезненных суставов. При анализе суставного синдрома при
ПсА обращали внимание на наличие параартикулярных проявлений и функцию
позвоночника и определяли симптомы Форестье, Отта, Шобера, Томайера,
Кушелевского (1,2,3), ограничение дыхательных экскурсий грудной клетки,
позвоночный индекс, индекс активности
BASDAI
(A.
Calin et al,
1999). Диагноз псориаза устанавливался дерматологом. При наличии показаний
больные осматривались окулистом. Для оценки функциональных возможностей и
качества жизни пациентов применяли опросник
HAQ
(J.
R.
Kirwan et al,
1986), HAQ-AS
(Lawren H.
Daltroy et al,
1990), функциональный тест
Lee и опросник
SF
36 (J.E.J.
Ware et al,
1992). Выраженность клинического эффекта у больных РА оценивали по динамике
ACR
критериев >20%, 50%, 70% улучшения (D.T.
Felson et al,
1995) включающих: a)
счет припухших суставов, б) счет болезненных суставов, в) улучшение по крайней
мере 3 из 5 показателей: 1) Общая оценка активности по мнению пациента. 2) Общая
оценка активности по мнению врача. 3) Оценка пациентом боли. 4) Острофазовые
показатели (СОЭ, СРБ). 5)
HAQ. Выраженность клинического эффекта у
больных РА оценивали также по влиянию проводимой терапии на индекс тяжести (М.
М. Иванова и др., 1994) и индекс активности
DAS
28. Выраженность клинического эффекта у больных ПсА оценивали по динамике
ACR
критериев (20%, 50%, 70%), адаптированных для ПсА (P.J.Mease
et al, 2000) и с помощью
PsARC
критериев (D.O.
Clegg,
1996), которые включали улучшение в двух из следующих четырех критериев, один
из которых должен быть болезненные и припухшие суставы и при этом отсутствие
ухудшения других критериев: 1) общая оценка активности по мнению врача (по 5
бальной шкале); 2) общая оценка активности по мнению больного (по 5 бальной
шкале); 3) улучшение на 30% и более числа болезненных суставов; 4) улучшение на
30% и более числа припухших суставов. При анализе поддерживающей терапии
ремиссию заболевания оценивали по критериям АРА (1987г.).
Кроме клинической оценки суставного синдрома
использовали весь комплекс лабораторного обследования больных, как для активного
выявления противопоказаний, так и для контроля за возможными побочными
действиями. В этот комплекс были включены: общий анализ крови с подсчетом
тромбоцитов, биохимические исследования крови (СРБ иммунотурбометрическим
методом реактивами фирмы «Rosh-Швейцария»,
нормальный показатель до 10 мг/дл, фибриноген, общий белок и белковые фракции,
мочевина, креатинин, билирубин, АЛТ, АСТ, ГГТП, ЩФ), анализы мочи. Из
инструментальных методов в процессе обследования использовались: ЭКГ,
рентгенография грудной клетки, рентгенография суставов кистей и стоп в динамике
(каждые 6 месяцев) с оценкой стадии болезни по
Steinbroker
и оценкой рентгенологического прогрессирования по модифицированному методу Шарпа,
рентгенография илеосакральных суставов с оценкой стадии по
Kellgren,
рентгенография различных отделов позвоночника и других пораженных суставов по
показаниям, ЭхоКГ исследование и УЗИ органов брюшной полости и почек для
выявления экстраартикулярных проявлений и возможных побочных действий препаратов
по показаниям.
Иммунологические методы
1) Определение РФ: РФ определяли в сыворотке
крови иммунотурбометрическим методом на автоматическом биохимическом анализаторе
Cobas Integra
(Rosh
– Швейцария), реактивами PF
фирмы Rosh
– Швейцария. За положительный результат считали РФ > 20
ME/ml.
2) Определение концентрации сывороточных
иммуноглобулинов: Определение содержания сывороточных иммуноглобулинов классов
A,
M,
G
проводилось методом радиальной иммунодиффузии по
Mancini et.
al.
В контрольной группе (n=56)
показатели принимали следующие значения:
Ig A
(1,87±0,18г/л),
Ig G
(12,47±0,54
г/л), Ig M
(1,05±0,06г/л).
3) Определение циркулирующих иммунных
комплексов: Циркулирующие иммунные комплексы (ЦИК) в сыворотке крови определяли
методом преципитации в растворе полиэтиленгликоля (ПЭГ) по Haskown в модификации
Ю.А. Григорович и А.Н. Алферовой. В контрольной группе доноров (n=24)
показатели ЦИК: 52,8±4,5
ед.опт.пл.
Определение стабильных метаболитов оксида
азота
Стабильные метаболиты оксида азота определяли в
сыворотке крови и моче методом спектрофотометрии с реактивом Грисса. В
контрольной группе (n=35)
показатели содержания стабильных метаболитов оксида азота в сыворотке крови: 4,2
± 0,78 мкг/л, в моче: 2,1 ± 0,45 мкг/л.
Статистическая обработка
полученных результатов проводилась с использованием ППП “Statistica
for Windows 5.0”. По каждому признаку
определяли среднюю величину (X)
и среднее квадратичное отклонение (s).
Изучение динамики исследуемых показателей в процессе лечения проводили с
помощью критерия Стьюдента с поправкой по Бонферрони и χ2. Во всех
случаях нулевую гипотезу отвергали при
p<0,05.
ПОЛУЧЕННЫЕ РЕЗУЛЬТАТЫ И ИХ ОБСУЖДЕНИЕ
1.
Сравнительный анализ клинической эффективности комбинированной
терапии проспидином и метотрексатом и монотерапии проспидином при РА
Исследование проведено у 137 больных с
неблагоприятными вариантами достоверного РА. 75 больных получали
комбинированную терапию проспидином и метотрексатом, 62 - проспидин. Группы
больных были вполне сопоставимы по основным клиническим показателям. В обеих
группах преобладали женщины с генерализованным суставным синдромом,
серопозитивные по РФ, имеющие системные проявления, с высокой или умеренной
степенью активности болезни, около трети больных имели стероидозависимость.
Комбинированная терапия проспидином и метотрексатом назначалась как описано
ранее. Доза проспидина для монотерапии была рассчитана исходя из суммарной
недельной дозы препарата (500 мг), обладающей клинической эффективностью.
Частота введения 1 раз в 5 дней
N
4-5 на стационарном этапе до достижения клинического улучшения.
Поддерживающая терапия проводилась в дозе 500 мг в месяц внутривенно капельно
на 200 мл 5% глюкозы, при нарастании активности дозу увеличивали до 1500-2000
мг в месяц.
Сравнительный анализ клинической
эффективности комбинированной терапии проспидином и метотрексатом и монотерапии
проспидином показал, что комбинированная терапия в указанном режиме, также как
и монотерапия проспидином, приводила к раннему клиническому эффекту (уже на
3-4 неделе терапии), но по сравнению с монотерапией проспидином, оказывала более
выраженный клинический эффект на всех этапах наблюдения (таблица 1).
Клиническая эффективность по критериям
ACR
20%, 50% и 70% составляла через 1 месяц лечения 92,9%, 58,6% и 25,7%
соответственно, а на протяжении исследования через год – 95,4%, 58,5%, 27,7%.
Таблица 1
Оценка общих результатов лечения в процессе
применения
комбинированной терапии проспидином и
метотрексатом и монотерапии проспидином у больных РА (ACR
критерии)
|
Сроки наблюдения,
количество больных |
1 мес.
(n-70/62)
|
3 мес.
(n-69/60)
|
6 мес.
(n-66/59)
|
12
мес.
(n-65/47)
|
|
ACR>20%
|
65 (92,9%)
49 (79%)
р=0,04 |
65 (94,2%)
48 (80,0%)
р=0,03 |
62 (93,9%)
46 (78,0 %)
р=0,019 |
62 (95,4%)
34 (72,3%)
р=0,002 |
|
ACR>50%
|
41 (58,6%)
30 (48,4%)
р=0,32 |
27 (39,1%)
20 (33,3%)
р=0,62 |
34 (51,5%)
27 (45,7%)
р=0,64 |
38 (58,5%)
21 (44,7 %)
р=0,211 |
|
ACR>70%
|
18 (25,7%)
13 (21,0%)
р=0,66 |
14 (20,3%)
5 (8,3%)
Р=0,096 |
20 (32,3%)
11 (18,6%)
р=0,19 |
18 (27,7%)
7 (14,9%)
р=0,169 |
|
Нет эффекта
|
5 (7,1%)
13 (21,0%)
р=0,04 |
4 (5,8%)
12 (20,0%)
р=0,03 |
4 (6,1%)
13 (22,0%)
р=0,019 |
3 (4,6%)
13 (27,7%)
р=0,002 |
Примечание: В числителе комбинированная терапия
проспидином и метотрексатом (1 группа), в знаменателе – проспидин (2 группа);
р- достоверность различий в группах по χ2.
В процессе наблюдения отсутствие эффекта (ACR<20%)
наблюдалось всего лишь у 4,6-7,1% больных, получавших комбинированную терапию,
и у 20-27,7% больных, получавших монотерапию проспидином. Из клинических
особенностей пациентов, резистентных к лечению можно было отметить: длительный
стаж болезни (более 8 лет), системные проявления и стероидозависимость.
Частота клинико-лабораторной ремиссии
в группе больных, получавших комбинированную терапию, была также выше (18,7%),
чем в группе монотерапии проспидином (12%). Из клинических показателей,
оказывающих положительное влияние на развитие ремиссии, в обеих группах больных
были отмечены: небольшой стаж болезни (до трех лет), отсутствие
стероидозависимости и системных проявлений заболевания.
Раннему и длительному улучшению клинических
показателей ревматоидного воспаления соответствовала и положительная динамика
СОЭ, СРБ, фибриногена, РФ и ЦИК в процессе лечения. Причем, наиболее
последовательное и достоверное снижение уровня лабораторных и иммунологических
показателей ревматоидного воспаления наблюдалось на фоне комбинированной
терапии. Снижение титров РФ было отмечено у 54% серопозитивных больных в группе
комбинированной терапии и у 36% серопозитивных больных в группе монотерапии
проспидином. Отсутствие РФ в сыворотке крови, или его персистенция, на фоне
проводимой комбинированной терапии регистрировалась у 20-22% больных и у 8-10% в
группе больных, получавших проспидин.
Под влиянием обоих способов лечения
удалось добиться положительной динамики со стороны системных проявлений. Такие
системные проявления как, лихорадка и лимфаденопатия исчезали после 3-4
введения препаратов в обеих группах. Всего под влиянием комбинированной терапии
купированы 83,5% системных проявлений и 60,9% - под влиянием терапии
проспидином.
Отрицательной динамики
рентгенологических изменений у большинства больных, продолжавших лечение в
течение всего срока наблюдения, в обеих группах не отмечено. Переход в более
тяжелую стадию (из I
во II,
из II
в III)
произошел у 8 больных (по 4 из каждой группы) на 6-12 месяце наблюдения. В
анамнезе у этих пациентов отмечалась резистентность и к другим видам базисной
терапии.
Снижение дозы ГКС и НПВС на фоне любой базисной
терапии считается одним из важных показателей эффективности терапии. В нашем
исследовании комбинированная терапия проспидином и метотрексатом, по сравнению с
монотерапией проспидином, чаще приводила к снижению суточной дозы и отмене НПВС
(рис. 1). Как видно из рис. 1, снизить суточную потребность в НПВС под
влиянием комбинированной терапии без ущерба для общих результатов лечения
удалось у 84,6% больных РА. Причем у 12,3% больных – на 15-25% от исходной,
у 26,2% больных - на 30-50%, у 29,2% больных - на 50% и более, а у 16,9%
больных НПВС удалось отменить полностью.
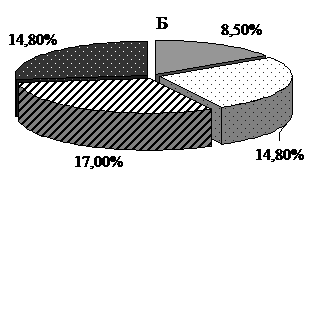 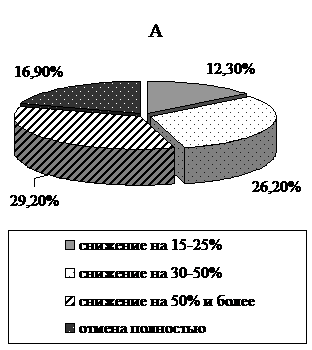
Рис. 1. Влияние
комбинированной терапии проспидином и метотрексатом (А) и монотерапии
проспидином (Б) на суточную потребность в НПВС у больных РА.
Комбинированная терапия проспидином и
метотрексатом, по сравнению с монотерапией проспидином, позволяла в два раза
чаще отменять преднизолон в случае стероидозависимости (рис. 2).
 
Рис. 2. Влияние комбинированной терапии
проспидином и метотрексатом (А) и терапии проспидином (Б) на суточную
потребность в стероидах у больных РА.
Максимальное положительное влияние на
стероидозависимость оба способа лечения оказывали на 3-6 месяце лечения (90%). В
процессе дальнейшего наблюдения изменение дозы происходило заметно реже.
В целом комбинированная терапия
проспидином и метотрексатом, по сравнению с монотерапией проспидином, позволяла
лучше контролировать активность болезни в процессе поддерживающей терапии,
оказывая более стабильное влияние на клинические и лабораторные показатели
ревматоидного воспаления, не повышая частоту побочных действий и связанных с
ними отмен. Побочные действия возникали примерно у трети больных в обеих группах
(29,3% и 26,3%) и лишь у половины из них они требовали отмены (13,3% и
11,2%). Появления ранее неизвестных побочных эффектов при приеме
комбинированной терапии проспидином и метотрексатом отмечено не было. В обеих
группах возникали побочные действия со стороны периферической нервной системы (парастезии,
повышенная чувствительность к холоду), дизурические явления, преходящая
протеинурия, церебральные расстройства, характерные для проспидина. В группе
больных, получавших комбинированную терапию, регистрировались также побочные
действия, типичные для метотрексата: диспепсия (тошнота, рвота), повышение
активности печеночных ферментов.
2.
Сравнительный анализ клинической эффективности
комбинированной терапии проспидином и метотрексатом
и монотерапии метотрексатом при РА
Сравнительный анализ проводили у 151 больного достоверным
РА. 75 больных получали комбинированную терапию проспидином и метотрексатом, 76
больных – монотерапию метотрексатом. Группы были сопоставимы по основным
клиническим и демографическим показателям. Комбинированную терапию проспидином и
метотрексатом применяли по методике, описанной в разделе материал и методы
исследования. Метотрексат назначали в дозе 10 мг в неделю в/м, поддерживающая
терапия проводилась в той же дозе. Доза метотрексата для монотерапии была
выбрана как достаточно эффективная и наименее токсичная. Оценку клинической
эффективности и лабораторное исследование проводили в начале и конце
стационарного этапа лечения, через 3, 6, 12, 18, 24, 36 месяцев поддерживающей
терапии.
2.1 Клинические аспекты
В процессе проводимой терапии в обеих
группах происходила положительная динамика клинических показателей, отражающих
выраженность суставного синдрома. Лечение в стационаре и длительная
поддерживающая комбинированная терапия и монотерапия метотрексатом приводили к
положительной динамике суставной
индекса, боли по ВАШ, количества болезненных, припухших суставов,
длительности утренней скованности на всех этапах наблюдения. Рассматривая
динамику этих показателей во времени можно отметить различные сроки появления
клинического эффекта. В случае применения комбинированной терапии, по отношению
к группе больных, получавших монотерапию метотрексатом, клинический эффект
развивался раньше (конец 3-ей, начало 4-ой недели лечения), а к концу
стационарного этапа лечения был уже, как правило, выражен. Быстрота наступления
клинического эффекта на фоне комбинированной терапии проспидином и
метотрексатом на ранних этапах лечения, очевидно, связана с самостоятельным
противовоспалительным действием проспидина, а нарастание эффекта в отдаленные
сроки с его иммунодепрессивными (антипролиферативными) свойствами, способностью
подавлять неоангиогенез и началом действия метотрексата. Положительная динамика
клинических показателей под влиянием комбинированной терапии сохранялась в более
поздние сроки наблюдения (18 - 36 мес.).
Соответственно положительной динамике
клинических показателей в процессе лечения проспидином и метотрексатом нами
установлена нормализация (или улучшение) лабораторных показателей: СОЭ, СРБ,
уровня фибриногена. Иммуномодулирующее, преимущественно иммунодепрессивное и
антипролиферативное действие данной комбинации проявлялось в снижении титров РФ,
ЦИК и иммуноглобулинов. Достоверное снижение уровня ЦИК, иммуноглобулинов
A,
М и G
(p<0,05)
наблюдалось к 3-6 месяцу комбинированной терапии и сохранялось на этапах
наблюдения 18, 24 и 36 месяцев. Наиболее последовательно отражала эффект
комбинированной терапии динамика показателей РФ, достоверное снижение которого
отмечалось достаточно рано (к концу стационарного этапа лечения). Снижение и
нормализация РФ продолжалась и в более поздние сроки наблюдения. Причем при
хороших результатах лечения чаще отмечалось снижение уровня РФ, при
незначительных – отсутствие динамики показателя, а обострение болезни обычно
соответствовало повышению уровня РФ. По сравнению с комбинированной терапией,
на фоне монотерапии метотрексатом позитивная динамика СОЭ и РФ была менее
выражена на всех этапах наблюдения, а уровни ЦИК и иммуноглобулинов существенно
не менялись (p>0,05).
Нормализация в процессе лечения (или улучшение) некоторых лабораторных (СОЭ СРБ)
и иммунологических показателей (РФ, ЦИК), отражающих активность и тяжесть РА,
подтверждает эффективность проводимой комбинированной терапии, указывает на ее
базисный характер и соответствует результатам клинического эффекта.
При
оценке общих результатов лечения, с использованием унифицированных методов
оценки терапии (критериев
ACR) было выявлено, что улучшение по
критериям ACR
20% регистрировалось у 92,9% на стационарном этапе, у 95,4% к 12 месяцу лечения
и у 93,4% на 36 месяце комбинированной терапии проспидином и метотрексатом (рис.
3).
 Рис. 3. Динамика ACR
20% у больных РА под влиянием комбинированной терапии проспидином и
метотрексатом (П+МТ) и монотерапии метотрексатом (МТ).
Рис. 3. Динамика ACR
20% у больных РА под влиянием комбинированной терапии проспидином и
метотрексатом (П+МТ) и монотерапии метотрексатом (МТ).
В том числе
ACR
50 и 70% наступало у 58,6% пациентов на стационарном этапе и сохранялось у 58,5%
больных к 12 месяцу комбинированной терапии проспидином и метотрексатом и у
52,5% - к 36 месяцу лечения (рис. 4). В сравнении с комбинированной терапией,
общие результаты лечения в группе монотерапия метотрексатом были хуже:
улучшение на уровне ACR
20% наблюдалось у 40% больных на стационарном этапе и у 76,9% пациентов в
процессе поддерживающей терапии. Монотерапия метотрексатом, по сравнению с
комбинированной терапией, реже приводила к значительному улучшению (ACR
50 и 70%) на всех этапах наблюдения (рис.4). Клинический эффект от
комбинированной терапии проспидином и метотрексатом отсутствовал всего у 3-5
(4,6%-6,6%) больных на каждом из этапов наблюдения, что гораздо реже, чем в
группе монотерапии метотрексатом (от 23% к 36 месяцу до 60% на стационарном
этапе). У больных с отсутствием эффекта от комбинированной терапии в течение
6-8 недель доза проспидина увеличивалась на 100 мг/неделю и проводилась
локальная терапия ГКС.
 Рис.
4. Динамика ACR
50% у больных РА под влиянием комбинированной терапии проспидином и
метотрексатом (П+МТ) и монотерапии метотрексатом (МТ). Рис.
4. Динамика ACR
50% у больных РА под влиянием комбинированной терапии проспидином и
метотрексатом (П+МТ) и монотерапии метотрексатом (МТ).
Анализ
исходных экстраартикулярных проявлений болезни установил, что чаще других
регистрировались полинейропатия, анемия, похудание, лихорадка. Они по-разному
реагировали на терапию. Наиболее чувствительными к действию проспидина и
метотрексата были: анемия, лихорадка, лимфаденопатия, похудание, ревматоидные
узлы, эписклерит и синдром Шегрена. На полинейропатию и кожный васкулит
лечение влияния не оказало. При изучении динамики экстраартикулярных проявлений
у больных, получавших лечение, нами было отмечено, что на первом году
комбинированной терапии исчезает большинство (87,1%) экстраартикулярных
проявлений болезни. Причем, в дальнейшем их рецидивов не наблюдается.
Монотерапия метотрексатом реже (50,8%) приводила к купированию системных
проявлений РА. Способность комбинированной терапии проспидином и метотрексатом
купировать большинство экстраартикулярных проявлений РА, может косвенно
свидетельствовать об иммунодепрессивной и антипролиферативной направленности
указанной комбинации, а, следовательно, и о ее патогенетической направленности
и базисных свойствах.
Одним из достоинств комбинированной
терапии проспидином и метотрексатом считали ее способность вызывать ремиссию,
различную по длительности и срокам наступления, что позволяет отнести эту
комбинацию к разряду базисных. Ремиссия длительностью от 3 до 18 месяцев была
установлена у 14 (18,7%) больных, получавших комбинированную терапию проспидином
и метотрексатом. Среди этих больных ремиссия длительностью 3 месяца наблюдалась
у 3 больных, 5 месяцев – у 1 больного, 6 месяцев – у 3, 9 месяцев у 3, 12
месяцев – у 2, 18 месяцев – у 2. На фоне ремиссии больные продолжали получать
проспидин в дозе 100 мг 1 раз в неделю и метотрексат 10 мг в неделю. Среди
всех больных, у которых развилась ремиссия, у 7 пациентов стаж РА был менее 2
лет, когда комбинированная терапия назначалась в качестве первого базисного
препарата. Монотерапия метотрексатом в нашем исследовании, по сравнению с
комбинированной терапией, реже (10,5%) приводила к ремиссии заболевания:
ремиссия была зарегистрирована у 8 больных (длительностью 3 месяца – у 2, 6
месяцев – у 4, 9 месяцев – у 1, 12 месяцев – у 1). Следует отметить, что
более ранняя и длительная ремиссия наблюдалась у больных со стажем РА менее 2
лет, с ранним началом базисной терапии (в течение первых 3-4 месяцев после
постановки диагноза).
Снизить суточную потребность в НПВС без
ущерба для общих результатов терапии в первый год лечения удалось у 55 больных
РА, получавших комбинированную терапию проспидином и метотрексатом. Причем, у
12,3% больных - на 15-25% от исходной, у 26,2% – на 30-50%, у 29,2% – на 50% и
более, у 11 пациентов (16,9%) НПВС удалось отменить полностью. Длительная (36
месяцев) поддерживающая комбинированная терапия приводила к снижению суточной
потребности в НПВС у 55,7% пациентов и позволяла отменить их полностью у
19,7%. Уменьшить суточную потребность в НПВС на первом году лечения
метотрексатом удавалось у 43,6%, к 24 месяцу – у 50%, к 36 месяцу – у 44,3%
больных, а более чем у половины пациентов доза НПВС оставалась неизменной.
Комбинированная терапия проспидином и метотрексатом оказала
положительное влияние и на стероидозависимость у 20 из 23 больных РА. При этом у
10 пациентов удалось уменьшить дозу ГКС на 30-50% от исходной, а у 5 больных,
получавших небольшие (5-10 мг) поддерживающие дозы преднизолона их полностью
отменить на фоне положительной динамики показателей ревматоидного воспаления. Монотерапия
метотрексатом у 4 больных из 14 выявляла нестабильность клинического эффекта в
отношении суставного синдрома, что требовало повышения суточной дозы
преднизолона. Снизить суточную дозу преднизолона в группе монотерапии
метотрексатом удалось у 3 больных на 12 месяце лечения, у 1 больного на 24
месяце и еще у 1 больного на 36 месяце.
Важным компонентом внедрения новых способов
рациональной базисной терапии является оценка ее переносимости, осложнений и
побочных действий, ведущих к ее отмене. Переносимость комбинированной терапии
проспидином и метотрексатом в нашем исследовании была вполне удовлетворительной
и по сравнению с монотерапией метотрексатом не приводила к нарастанию частоты
побочных действий и связанных с ними отмен (таблица 2).
Таблица 2
Побочные действия и частота
отмены в процессе применения комбинированной терапии проспидином и
метотрексатом и монотерапии
метотрексатом у больных РА.
|
Побочные действия |
Количество больных (%) |
|
П+МТ |
МТ |
|
Парестезии |
6,7 (2,6) |
- |
|
Дизурические явления |
2,7 |
- |
|
Преходящая протеинурия (до
0,6-0,9 г/л) |
2,7 |
- |
|
Головокружение, слабость,
гипотония |
4 (4) |
- |
|
Аллергический дерматит |
1,3 (1,3) |
2,6 (2,6) |
|
Нарушения менструального цикла |
4 |
5,2 (1,3) |
|
Преходящая азотемия |
1,3 (1,3) |
- |
|
Диспепсические расстройства |
5,3 |
7,9 |
|
Повышение активности печеночных
ферментов |
5,3 (4) |
9,2 (6,6) |
|
Анемия |
- |
2,6 (2,6) |
|
Язвенный стоматит |
- |
2,6 (2,6) |
|
Алопеция |
- |
2,6 (2,6) |
|
Всего: |
33,3 (18,6) |
32,7 (18,3) |
Примечание: в скобках – частота отмены.
Появления ранее неизвестных побочных действий
при приеме комбинированной терапии выявлено не было. В основном регистрировались
нетяжелые побочные действия. Самыми частыми из них были побочные действия со
стороны периферической нервной системы: парестезии, повышенная чувствительность
к холоду и дизурические явления, которые в большинстве случаев проходили
самостоятельно после снижения дозы проспидина или увеличения интервала между его
введениями. Из тяжелых побочных действий были отмечены церебральные расстройства
в виде головокружения, гипотонии, общей слабости, развитие аллергического
дерматита, повышение креатинина, повышение активности печеночных ферментов более
чем в 3 раза и диспепсические расстройства, что послужило поводом для отмены
терапии у 18,6% больных (таблица 2). Максимальное количество отмен препаратов
(у 9 больных) в связи с побочными эффектами было отмечено в первые 6 – 9 месяцев
лечения.
2.2. Влияние комбинированной терапии проспидином
и метотрексатом и монотерапии метотрексатом
на рентгенологическое прогрессирование у больных РА
К важным параметрам, отражающим эффективность
базисных противоревматических препаратов, относится их влияние на выраженность
рентгенологического прогрессирования деструкции суставов. В целом по
данным литературы оценка влияния метотрексата на темпы рентгенологического
прогрессирования при РА до сих пор окончательно не определена. В нашем
исследовании терапия низкими дозами метотрексата по динамике общего количества
эрозий и коэффициентам костной и хрящевой деструкции не замедляла темпы
рентгенологического прогрессирования в течение 3-х летнего периода наблюдения
(табл. 3).
Таблица 3
Показатели костной и хрящевой деструкции у
больных РА под воздействием комбинированной терапии и монотерапии метотрексатом
(X±s).
|
Этапы наблюдения |
Коэффициент костной деструкции |
Коэффициент хрящевой деструкции |
|
6 месяцев
|
0,64±0,21
0,63±0,33 |
5,6±2,64
2,4±1,32 |
|
12 месяцев
|
0,38±0,17***
0,65±0,46
p# |
3,6±1,76***
2,4±1,2
p# |
|
18 месяцев
|
0,33±0,13***
0,68±0,41
p# |
2,86±1,55***
2,5±0,9 |
|
24 месяцев
|
0,31±0,11***
0,72±0,4
p# |
2,58±1,48***
2,6±0,6 |
|
36 месяцев
|
0,27±0,12***
0,78±0,29
p# |
2,2±1,43***
2,8±0,56
p# |
Примечание:
в числителе – комбинированная терапия, в знаменателе – монотерапия метотрексатом.
Достоверность показателей по отношению к исходным: ***-р<0,001;
p# - достоверность различия между 1 и 2 группами (во
всех случаях р<0,001).
При оценке динамики рентгенологических изменений в течение 36
месяцев непрерывной комбинированной терапии проспидином и метотрексатом, по
сравнению с монотерапией метотрексатом, не было выявлено достоверной тенденции к
увеличению количества вновь образованных эрозий (р>0,05), а к 12 месяцу лечения
наблюдалось снижение среднего прироста эрозий более чем в 2,5 раза (рис.5) и
достоверное снижение динамики коэффициента костной и хрящевой деструкции (табл.
3).

Рис. 5. Средний прирост
эрозий у больных РА, получавших комбинированную терапию проспидином и
метотрексатом (П+МТ) и монотерапию метотрексатом (МТ).
Переход в более тяжелую стадию с развитием эрозивного процесса в суставах
кисти был выявлен у 7 больных, получавших монотерапию метотрексатом, и у 4
больных (у 2 больных из II в III
, и еще у 2 из I во II
стадию болезни) в группе комбинированной терапии на этапе 6-9 месяцев лечения.
Из клинических особенностей в анамнезе у этих пациентов отмечалось отсутствие
эффекта и от других видов базисной терапии.
2.3. Влияние комбинированной терапии проспидином
и метотрексатом и монотерапии метотрексатом на функциональный
статус и качество жизни у больных РА
Важными критериями оценки эффективности проводимой терапии
являются показатели функционального статуса и качество жизни больных РА. Оценку
изучаемых параметров проводили при помощи опросника состояния здоровья
HAQ, теста Lee и
SF-36. Кроме того, в процессе лечения проводили оценку
индекса тяжести, косвенно отражающего функциональные способности пациентов, так
как в его состав входят степень функциональной недостаточности больного и
показатели активности болезни. При этом были получены следующие результаты. Под
влиянием комбинированной терапии проспидином и метотрексатом и монотерапии
метотрексатом наблюдалась положительная динамика показателей, отражающих
функциональный статус больных, а также индекса тяжести. Тем не менее,
комбинированная терапия проспидином и метотрексатом, по сравнению с монотерапией
метотрексатом, приводила к более быстрому и выраженному улучшению показателей
теста Lee, HAQ (рис. 6).
Улучшение функциональных показателей на фоне терапии проспидином и метотрексатом
наступало уже к концу стационарного этапа лечения и сохранялось на этом уровне
при дальнейшем наблюдении (рис. 6).
 Рис. 6. Динамика HAQ под влиянием комбинированной
терапии проспидином и метотрексатом (П+МТ) и монотерапии метотрексатом (МТ) у
больных РА.
Рис. 6. Динамика HAQ под влиянием комбинированной
терапии проспидином и метотрексатом (П+МТ) и монотерапии метотрексатом (МТ) у
больных РА.
Средний индекс тяжести на момент начала комбинированной терапии
составлял 6,3 балла. За время комбинированной терапии проспидином и
метотрексатом происходило уменьшение индекса тяжести на 45%. В то время как
монотерапия метотрексатом снижала индекс тяжести на 16%.
Нами
проведено исследование воздействия заболевания и проводимого лечения на
показатели физического, психологического и социального функционирования больных.
Все показатели качества жизни были достоверно значимо хуже у больных РА в
сравнении со здоровыми лицами (p<0,001). При этом
самые низкие показатели качества жизни у больных РА были получены до начала
лечения. Комбинированная терапия улучшала параметры качества жизни больных
РА: улучшалось физическое, психологическое состояние больных, а также их
социальная адаптация. При этом комбинированная терапия, по сравнению с
монотерапией метотрексатом, достоверно улучшала все параметры качества жизни уже
на стационарном этапе (p<0,05). Улучшение показателей
качества жизни, достигнутое в течение 4-х недель, сохранялось длительно до
3-х лет. В группе больных, получавших монотерапию метотрексатом, результаты
оценки показателей физического здоровья (физическое функционирование, ролевое
физическое функционирование, боль) схожи: имеется достоверное улучшение (p<0,05).
Достоверного изменения показателей психологического здоровья, социального
функционирования, жизнеспособности и общего здоровья, по сравнению с
показателями до лечения, на фоне монотерапии метотрексатом мы не наблюдали.
3.
Клинический анализ эффективности комбинированной терапии
проспидином и метотрексатом у больных ранним РА
и установленным стабильным РА
Изучая клиническую эффективность
комбинированной терапии проспидином и метотрексатом у больных ранним РА,
сравнивали группу больных со стажем болезни до 1 года (n-28)
и группу пациентов с длительностью суставного синдрома более 1 года (n-47).
Группы были сопоставимы по полу, возрасту, наличию РФ и степени активности, но
различались по длительности болезни и рентгенологической стадии.
Комбинированная терапия у больных
ранним РА, по сравнению с больными со стажем болезни более 1 года, приводила к
более выраженному снижению суставного индекса, боли по ВАШ, количества
болезненных и припухших суставов и длительности утренней скованности на всех
этапах наблюдения. К концу 1-го месяца терапии 57,1% больных с ранним РА
имели низкую активность (DAS
28<3,2) в сравнении с 14,3% больных со стажем болезни более 1 года. В
дальнейшем, число больных с низкой активностью по
DAS
28 у больных ранним РА увеличивалось и к 12 месяцу лечения 60,9% пациентов
имели DAS
28<3,2 по сравнению с 45,2% больных со стажем болезни более 1 года.
При оценке общих результатов лечения по
ACR
критериям комбинированная терапия проспидином и метотрексатом у больных ранним
РА приводила к значительному улучшению (ACR
50 и 70%) у 85,7% больных на стационарном этапе, которое сохранялось в ходе
поддерживающей терапии у 82,6% пациентов (рис. 7).
Общие результаты лечения у больных со
стажем болезни более 1 года были значительно хуже: улучшение на уровне
ACR
50 и 70% на 1 месяце лечения наблюдалось у 40,5%, к 12 месяцу – у 45,2% больных
(рис. 7).
Отсутствие эффекта (ACR<20%)
в группе больных ранним РА было отмечено у 1 больного на стационарном этапе и у
1 пациента к 12 месяцу наблюдения. Отсутствие эффекта у больных со стажем
болезни более 1 года регистрировалось несколько чаще: у 4 больных на 1,3 и 6
месяце и у 2 пациентов на 12 месяце наблюдения.
Комбинированная терапия у больных
ранним РА чаще (25%) приводила к ремиссии заболевания, чем у пациентов с
длительным стажем болезни (14,9%). Кроме того, ремиссия при раннем РА была более
длительная (от 6 до 18 месяцев) и возникала быстрее (на этапах наблюдения 1 –
3 месяца).
 Рис. 7. Динамика ACR
50 и 70% у больных РА со стажем болезни до 1 и более 1 года под влиянием
комбинированной терапии проспидином и метотрексатом.
Рис. 7. Динамика ACR
50 и 70% у больных РА со стажем болезни до 1 и более 1 года под влиянием
комбинированной терапии проспидином и метотрексатом.
Анализ рентгенологических изменений в
сравниваемых группах больных через 12 месяцев показал, что комбинированная
терапия приводила к достоверному снижению коэффициента костной и хрящевой
деструкции (p<0,001)
у больных ранним РА. У больных РА со стажем болезни более 1 года наблюдалась
тенденция к снижению коэффициента костной деструкции и достоверное снижение
коэффициента хрящевой деструкции. Достоверного увеличения количества эрозий не
наблюдалось в обеих группах. Положительное влияние проводимой терапии на
изменения рентгенологических показателей наблюдалось уже к 6 месяцу лечения и
сохранялось на сроке 12 месяцев.
Комбинированная терапия проспидином и
метотрексатом у больных ранним РА приводила к более выраженному улучшению
показателей функционального статуса:
HAQ
2,64±1,67 – 0,87±0,8 (в сравнении с больными со стажем болезни более 1 года:
2,8±0,88 – 1,34±0,9), тест
Lee
15,9±6,4 – 5,11±4,9 (соответственно 16,19±5,1 – 7,06±5,0).
Показатели физического и
психологического здоровья в процессе комбинированной терапии улучшались в обеих
группах (p<0,05),
но в группе с длительным стажем болезни они оставались более низкими, чем у
больных ранним РА.
4. Сравнительный анализ комбинированной
терапии проспидином
и метотрексатом и монотерапии метотрексатом
при раннем РА
Сравнительный анализ проведен у 63 больных
ранним РА в открытом контролируемом 12 месячном исследовании. 28 больных
получали комбинированную терапию проспидином и метотрексатом (I
группа), 35 больных - монотерапию метотрексатом (II
группа). Группы больных были сопоставимы по основным демографическим и
клиническим показателям. Преобладали женщины (25 и 33 соответственно) 4-5
десятилетия жизни. Все больные имели длительность заболевания не более 1 года,
генерализованный суставной синдром и высокую степень активности. Большинство
больных были серопозитивны по РФ (22 и 34) и имели системные проявления (21 и
25).
Комбинированная терапия проспидином и
метотрексатом, по сравнению с монотерапией метотрексатом, оказывала более
быстрое (4 неделя лечения) и выраженное влияние на суставной индекс, боль по
ВАШ, число болезненных и припухших суставов, длительность утренней скованности.
Оба способа лечения оказали положительное
влияние на системные проявления у больных ранним РА. Комбинированная терапия,
по сравнению с монотерапией МТ, приводила к исчезновению большинства (19 из 33)
экстраартикулярных проявлений РА уже на 1-м месяце лечения. Применение
только метотрексата позволило купировать на стационарном этапе лечения только
9 из 25 системных проявлений. К 12 месяцу наблюдения в группе больных
комбинированной терапии регистрировались 5 системных проявлений из 33, в группе
больных монотерапии метотрексатом – 17 из 25.
В обеих группах больных произошла положительная
динамика основных лабораторных и некоторых иммунологических показателей. Но на
фоне комбинированной терапии, по сравнению с монотерапией метотрексатом,
наблюдалось более выраженное снижение СОЭ (p<0,001)
, СРБ (p<0,001),
РФ (p<0,001),
ЦИК (p<0,05)
и иммуноглобулинов (p<0,05)
на всех этапах наблюдения, что соответствовало общим результатам лечения.
Согласно
ACR
- критериям ответа на лечение к 1 месяцу лечения комбинация проспидина с
метотрексатом была также более эффективна, чем только метотрексат. 96,4%
пациентов, получавших комбинированную терапию и имевших 20% и более улучшение
по ACR
критериям, достигли его за 4 недели, что демонстрирует быстрое начало действия
препаратов. При этом 85,7% пациентов в группе комбинированной терапии имели
улучшение на уровне ACR>50%
(рис. 8), а 35,7% больных - значительное улучшение (ACR>70%).
К концу 12 месяца лечения улучшение
ACR
более 20% сохранялось у 95,7% пациентов, получавших комбинированную терапию. Из
них ACR
50% и 70% наблюдалось у 82,6% пациентов.
Монотерапия метотрексатом приводила к более
скромным результатам лечения. На стационарном этапе лечения улучшение
ACR
20% было отмечено лишь у трети больных второй группы, у 65,7% пациентов к 1
месяцу лечения эффект отсутствовал (ACR<20%).
Улучшение по ACR–критериям
более 50% и 70% в группе монотерапии метотрексатом к концу 1 месяца лечения было
отмечено у 11,4% больных, к 12 месяцу - у 35,7% больных.
 Рис.
8. Динамика ACR
50 и 70% у больных ранним РА под влиянием комбинированной терапии проспидином и
метотрексатом (П+МТ) и монотерапии метотрексатом (МТ). Рис.
8. Динамика ACR
50 и 70% у больных ранним РА под влиянием комбинированной терапии проспидином и
метотрексатом (П+МТ) и монотерапии метотрексатом (МТ).
Комбинированная терапия проспидином и
метотрексатом, по сравнению с монотерапией метотрексатом, чаще приводила к
ремиссии заболевания (25% и 14,3% соответственно), оказывала более выраженное
влияние на показатели функционального статуса и качество жизни больных РА.
Результаты SF-36
показали, что пациенты, получающие комбинированную терапию проспидином и
метотрексатом, более энергичны, жизнеспособны и их социальная активность в
меньшей степени зависит от материальных и эмоциональных проблем. Причем,
улучшение функциональных способностей и качества жизни отмечалось при лечении
комбинированной терапией в течение года.
Снизить суточную потребность в НПВС удалось у
большинства больных (91,2%) в группе комбинированной терапии. Причем, у 30,4%
больных комбинированная терапия позволяла снизить дозу НПВС более чем на 50%, а
еще у 30,4% их полностью отменить. Снизить суточную потребность в НПВС на
фоне монотерапии метотрексатом удалось у 21,5% пациентов, из них снижение
суточной дозы более чем на 50% стало возможным у 3,6% больных, и еще у 3,6%
они были отменены.
У 3 из 7 стероидозависимых больных, получавших
комбинированную терапию, доза преднизолона была уменьшена на 50%, а еще у 2-х
пациентов удалось отменить его полностью. Из 5 стероидозависимых больных,
получавших только метотрексат, снизить дозу преднизолона на 50% удалось у 1
больного. 4 пациентам, получавшим монотерапию метотрексатом без эффекта, мы
были вынуждены назначить стероиды впервые.
При оценке показателей рентгенологического
прогрессирования через 12 месяцев лечения была отмечена задержка
прогрессирования заболевания на фоне комбинированной терапии. По сравнению с
монотерапией метотрексатом, комбинированная терапия не приводила к достоверному
увеличению количества эрозий и к 12 месяцу наблюдения в первой группе отмечалось
достоверное снижение не только коэффициента хрящевой, но и костной деструкции (p<0,001).
По частоте и тяжести побочных действий и
связанных с ними отмен, комбинированная терапия проспидином и метотрексатом у
больных ранним РА была вполне сопоставима с монотерапий метотрексатом.
Побочные действия были выявлены у 32,1% больных, получавших комбинированную
терапию и у 34,3% пациентов, получавших монотерапию метотрексатом. Во второй
группе наблюдались типичные для метотрексата побочные действия: диспепсические
расстройства, повышение активности печеночных ферментов, цитопения,
аллергический дерматит. В группе больных, получавших комбинированную терапию,
встречались побочные действия характерные для проспидина (парастезии, дизурия) и
метотрексата. Поводом для отмены лечения у больных, получавших только
метотрексат, послужили как побочные действия (20%), так и отсутствие эффекта
(14,2%). Комбинированную терапию отменили из-за лекарственной токсичности у
17,9% больных. Отмен лечения из-за отсутствия эффекта в первой группе не было.
4.
Сравнительный анализ клинической эффективности
комбинированной терапии проспидином и метотрексатом
и монотерапии метотрексатом при ПсА
Открытое контролируемое 12-месячное
исследование проведено у 63 больных достоверным ПсА. 30 больных получали
комбинированную терапию проспидином и метотрексатом (первая группа), 33 больных
– монотерапию метотрексатом (вторая группа). В обеих группах преобладали
женщины (21 и 21 соответственно). Средний возраст - 43,2±9,5 и 40,5±8,4 лет.
Длительность суставного синдрома - 4,8±4,7 и 4,7±5,7 лет. Стаж кожного псориаза
- 12,4±11,2 и 11,6±12,1 лет. Все они имели вульгарный очаговый (12 и 21) или
распространенный (18 и 12) псориаз в прогрессирующей (18 и 11) или стационарной
(11 и 22) стадии, полиартритический вариант суставного синдрома (63),
I-III
рентгенологические стадии. У 16 больных первой группы и у 22 больных 2-ой
группы был выявлен сакроилеит
III
стадии, у 10 в каждой группе – признаки спондилоартрита. Около трети больных в
исследуемых группах имели высокую степень активности и тяжелую форму болезни с
системными проявлениями в виде лихорадки, анемии, похудания, лимфаденопатии и
увеита (11 и 12).
Комбинированная терапия проспидином и
метотрексатом, по сравнению с монотерапией метотрексатом, приводила к быстрому
(1-ый месяц) и выраженному улучшению клинических показателей суставного
синдрома. При этом комбинированная терапия, по сравнению с монотерапией
метотрексатом, положительно влияла не только на пораженные периферические
суставы, но и на воспалительный процесс в осевом скелете. По сравнению с
монотерапией метотрексатом, на фоне комбинированной терапии происходило
достоверное уменьшение боли и выраженности утренней скованности в позвоночнике,
локальной болезненности. Монотерапия метотрексатом отчетливо не влияла на
течение воспалительного процесса в позвоночнике. Положительное влияние
комбинированной терапии, по сравнению с монотерапией метотрексатом, на
суставной синдром при ПсА подтверждают результаты оценки эффективности лечения
с использованием критериев
PsARC (рис. 9).
 Рис.
9. Общая оценка эффективности комбинированной терапии проспидином и
метотрексатом (П+МТ) и монотерапии метотрексатом (МТ) у больных ПсА (PsARC). Рис.
9. Общая оценка эффективности комбинированной терапии проспидином и
метотрексатом (П+МТ) и монотерапии метотрексатом (МТ) у больных ПсА (PsARC).
Как
видно из рис. 9, на стационарном этапе лечения в группе комбинированной
терапии проспидином и метотрексатом улучшение клинических показателей ПсА
соответствовало критериям PsARC у большинства больных
(71,4%). В то время как монотерапия метотрексатом приводила к улучшению согласно
данным критериям у 16,1% пациентов (χ2=16,23; р=0,001). В
дальнейшем, число больных, ответивших на PsARC-критерии
хотя и увеличивалось в обеих группах, но было все же выше в группе
комбинированной терапии.
Проводимая терапия в обеих группах способствовала исчезновению
большинства системных проявлений ПсА. На фоне комбинированной терапии удалось
купировать все системные проявления уже к концу 1-го месяца лечения. Рецидивов
системных проявлений в процессе поддерживающей терапии проспидином и
метотрексатом не наблюдалось. В группе больных, получавших монотерапию
метотрексатом, на стационарном этапе было купировано 11 из 26 (42,3%)
системных проявлений, а к концу 12-месячного курса лечения - 23 (88,5%).
Оба
способа лечения оказывали положительное влияние на течение кожного синдрома при
ПсА (рис. 10).
 
Рис. 10.
Влияние комбинированной терапии проспидином и метотрексатом (П+МТ) и
монотерапии метотрексатом (МТ) на течение кожного синдрома при ПсА, где А
-ограничение площади дерматоза, Б - эволюция прогрессирующей стадии в
стационарную, В - купирование кожного синдрома, Г- без изменений.
На фоне проводимой терапии отмечалось уменьшение площади
высыпаний, существенно уменьшалась инфильтрация кожи, бляшки становились
плоскими, полностью проходил кожный зуд. Однако следует отметить, что
комбинированная терапия проспидином и метотрексатом, по сравнению с монотерапией
метотрексатом несколько чаще приводила к эволюции прогрессирующей стадии
псориаза в стационарную и купированию кожного синдрома.
В
обеих группах на фоне терапии было зарегистрировано снижение уровня СОЭ, СРБ и
ЦИК. Однако, на фоне комбинированной терапии, по сравнению с монотерапией
метотрексатом, достоверное снижение (р<0,05) указанных показателей наблюдалось
уже на стационарном этапе лечения и сохранялось в процессе поддерживающей
терапии. Комбинированная терапия, по сравнению с монотерапией метотрексатом,
приводила также к достоверному (р<0,05) снижению уровня иммуноглобулинов А и
G к концу 3 месяца лечения и иммуноглобулина М к
концу 12 месяца терапии. Достоверного изменения уровней иммуноглобулинов на фоне
монотерапии метотрексатом не было выявлено.
В
таблице 4 представлено влияние способов лечения на темпы рентгенологического
прогрессирования у больных ПсА.
Таблица 4
Влияние комбинированной терапии и монотерапии метотрексатом на
рентгенологическое прогрессирование у больных ПсА (Х±σ).
|
Показатель |
Этапы наблюдения |
|
До леч.
n=30/33 |
6 мес.
n=25/29 |
12 мес.
n=25/22 |
|
Количество эрозий |
2,19±3,06
2,44±2,85
р#=0,738 |
2,28±3,22
3,5±4,1
p#=0,235 |
2,27±3,12
4,78±5,1*
p#=0,045 |
|
Количество эрозированных суставов |
1,65±2,47
1,72±2,03
p#=0,902 |
1,8±2,75
3,0±3,7
p#=0,188 |
1,82±2,66
4,11±4,6*
p#=0,04 |
|
Коэффициент динамики костной деструкции |
- |
0,19±0,24
0,52±0,56
p#=0,009 |
0,12±0,18
0,58±0,63
p#=0,001 |
|
Коэффициент динамики хрящевой деструкции |
- |
5,69±4,59
6,18±1,63
p#=0,593 |
3,62±1,88***
6,28±2,31
p#=0,0001 |
Примечание:
в числителе – проспидин + метотрексат, в знаменателе – метотрексат.
Достоверность по отношению к исходным показателям: * - р<0,05, *** - р<0,001;
p# - достоверность различия между 1 и 2 группами.
Как видно из таблицы 4, комбинированная терапия, по сравнению с монотерапией,
не приводила к достоверному увеличению количества эрозий и эрозированных
суставов за 12 месяцев наблюдения. Кроме того, в группе комбинированной терапии
было отмечено достоверное снижение коэффициента динамики хрящевой деструкции (р<0,001)
и тенденция к снижению коэффициента костной деструкции.
В целом оценка динамики рентгенологических изменений выявила стабилизацию
костных изменений в первые 6 месяцев у всех больных, в срок 6-12 месяцев – у
93,3% больных в группе комбинированной терапии. В группе монотерапии
метотрексатом стабилизация костных изменений наблюдалась у 87,9% пациентов в
первые 6 месяцев лечения и в срок 6-12 месяцев – у 81,8%. Переход в следующую
стадию болезни был отмечен у 12 (19%) больных на всех сроках наблюдения (у 2
больных на комбинированной терапии и у 10 больных на монотерапии). У всех этих
пациентов было тяжелое течение болезни, резистентное, в том числе к
комбинированной терапии у 2 больных и к терапии МТ у 6 больных, которые были
отменены в связи с неэффективностью.
Улучшение функционального теста Lee и
HAQ наблюдалось в обеих группах (таблица 5). Но в
группе комбинированной терапии, по сравнению с монотерапией метотрексатом,
было отмечено более раннее (уже на стационарном этапе) и выраженное улучшение
показателей теста Lee и HAQ
на всех этапах наблюдения.
Таблица 5
Динамика показателей функционального статуса у больных ПсА под влиянием
комбинированной терапии и монотерапии метотрексатом (X±σ).
|
Показатель |
Этапы наблюдения |
|
До леч.
n=30/33 |
1 мес.
n=28/31 |
3 мес.
n=27/30 |
6 мес.
n=25/29 |
12 мес.
n=25/22 |
|
Функциональный тест
Lee (баллы) |
14,7±5,1
15,0±4,3 |
7,4±5,3*
13,4±4,5
p# |
6,1±5,0*
12,9±4,4
p# |
5,3±5,2*
12,2±5,7
p# |
4,8±5,1*
11,5±5,4*
p# |
|
HAQ
(баллы) |
1,9±0,6
1,8±0,7 |
0,7±0,6*
1,5±0,7
p# |
0,6±0,5*
1,5±0,6
p# |
0,5±0,6*
1,2±0,7*
p# |
0,4±0,6*
1,3±0,6*
p# |
Примечание:
В числителе – проспидин + метотрексат (1 группа), в знаменателе – метотрексат (2
группа). * - достоверность различий по отношению к показателям до лечения по
критерию Стьюдента с поправкой Бонферрони; p# -
достоверность различия между 1 и 2 группами (во всех случаях р<0,001).
Полученные данные по качеству жизни и динамике отдельных показателей
качества жизни на фоне проводимой терапии позволяют утверждать, что в период
активности ПсА ухудшается качество жизни больных: страдает физическое,
психологическое здоровье, нарушается социальная активность. В нашем исследовании
оба способа лечения приводили к достоверному улучшению ряда показателей
физического здоровья (физического функционирования, ролевого физического
функционирования, боли) и ролевого эмоционального функционирования. Но влияние
комбинированной терапии на показатели физического здоровья было более
выраженным (р<0,001) и отмечалось уже на стационарном этапе. Достоверное
улучшение показателей психологического здоровья, общего здоровья и социального
функционирования наблюдалось только на фоне комбинированной терапии. В ходе
поддерживающей терапии влияние комбинированной терапии на физическое
функционирование, ролевое физическое функционирование, боль, ролевое
эмоциональное функционирование и психологическое здоровье также было более
заметным (р<0,001). Изменения показателей жизнеспособности не были
статистически достоверными в обеих группах. Но на фоне комбинированной терапии,
по сравнению с монотерапией метотрексатом, отмечалась их положительная
тенденция.
Дополнительным критерием эффективности лечения считали влияние терапии на
суточную потребность в НПВС. Снизить суточную потребность в НПВС удалось у 80%
больных в группе комбинированной терапии и у 40,9% пациентов в группе
монотерапии метотрексатом. Причем, у 24% больных, получавших комбинированную
терапию, суточная доза НПВС была снижена на 50% и более, а у 32% стало возможным
отменить их полностью. В группе монотерапии метотрексатом снизить суточную дозу
НПВС на 50% и более удалось у 13,6% пациентов, а отменить их полностью – у 9,1%
.
У 10 больных (у 7 из группы комбинированной терапии и у 3 из
группы метотрексата) была зарегистрирована ремиссия заболевания (от 3 до 9
месяцев). Все они имели стаж суставного синдрома не более 2-х лет. У 2-х
больных в группе комбинированной терапии ремиссия сохранялась в течение 9
месяцев. На фоне ремиссии больные продолжали принимать комбинированную терапию
проспидином иметотрексатом и монотерапию метотрексатом в поддерживающих дозах.
По сравнению с монотерапией метотрексатом, в группе комбинированной терапии
ремиссия заболевания регистрировалась существенно чаще (23,3% и 9,1%
соответственно).
Переносимость терапии в обеих группах была удовлетворительной
(таблица 6). К 12 месяцу монотерапию метотрексатом продолжали 22 больных из
33 (66,7%). Побочные действия отмечены у 12 больных (36,4%) и были типичными
для метотрексата: диспепсические расстройства, повышение уровня печеночных
ферментов, афтозный стоматит, аллергический дерматит, головокружение. У 5
больных (15,1%) эти побочные действия потребовали отмены. Еще у 6 больных
метотрексат был отменен в связи с отсутствием эффекта (18,2%).
Таблица 6
Побочные действия и частота отмены в процессе применения комбинированной терапии
и монотерапии метотрексатом у больных ПсА.
|
Побочные действия |
Проспидин+метотрексат, % |
Метотрексат, % |
|
Дизурия |
3,3 (3,3) |
- |
|
Парестезии |
3,3 |
- |
|
Головокружение |
3,3 |
3,0 (3,0) |
|
Диспепсические
расстройства |
3,3 |
15,1 (3,0) |
|
Повышение уровня
печеночных ферментов |
3,3 (3,3) |
12,1 (3,0) |
|
Афтозный стоматит |
- |
3,0 (3,0) |
|
Аллергический
дерматит |
3,3 (3,3) |
3,0 (3,0) |
|
Всего отмен
из-за лекарственной
токсичности: |
23,3 (10) |
36,4 (15,1) |
|
Отмена из-за
отсутствия эффекта |
6,7 (6,7) |
18,2 (18,2) |
Примечание: в скобках - частота отмены.
Комбинированная терапия проспидином и метотрексатом, по сравнению с монотерапией
метотрексатом, не приводила к нарастанию частоты побочных действий и связанных с
ними отмен (табл. 6). К 12 месяцу лечение комбинированной терапией проспидином и
метотрексатом получали 25 больных из 30 (83,3%), побочные действия были
выявлены у 7 больных (23,3%). В 2-х случаях наблюдалось повышения уровня
печеночных ферментов. Среди других побочных действий встречались: дизурия,
парастезии, головокружение, аллергический дерматит, диспепсические
расстройства. Поводом к отмене комбинированной терапии явились побочные
действия у 3 больных (10%) и резистентность к лечению у 2 больных (6,7%).
ВЫВОДЫ
1.
По результатам сравнительного контролируемого 36-месячного
изучения 276 больных РА и ПсА комбинированная терапия проспидином и
метотрексатом обладает быстрым (3-4 неделя лечения) и выраженным клиническим
эффектом, имеет хорошую переносимость, улучшает показатели функционального
статуса и качество жизни, замедляет темпы рентгенологического прогрессирования
через 12 месяцев непрерывной терапии, позволяет уменьшить суточную потребность в
НПВС и ГКС (в случае стероидозависимости), способна вызывать ремиссию.
2.
Комбинированная терапия проспидином и метотрексатом у больных РА, по
сравнению с монотерапией проспидином, чаще приводит к клиническому улучшению
(улучшение ACR 20% к 12 месяцу терапии наблюдалось у
95,4% и 72,3% больных соответственно; р=0,002), снижению суточной потребности в
НПВС и ГКС (в случае стероидозависимости) и ремиссии заболевания (у 18,7% и 12%
пациентов соответственно).
3.
По непосредственным и отдаленным результатам лечения комбинированная
терапия проспидином и метотрексатом превосходит монотерапию метотрексатом у
больных РА за счет более быстрого (на 3-4 неделе) и выраженного наступления
клинического эффекта (ACR
50% и 70% к 1 месяцу лечения наблюдалось у 58,6% и 11,4% больных соответственно,
р=0,001; к 36 месяцу - у 52,5% и 21,1%, р=0,006), более частого положительного
влияния на суточную потребность в НПВС и ГКС (в случае стероидозависимости) и
чаще вызывает ремиссию заболевания (18,7% и 10,5% соответственно).
4.
Комбинированная терапия проспидином и метотрексатом у больных РА, по
сравнению с монотерапией метотрексатом, не приводит к нарастанию частоты
побочных действий и связанных с ними отмен. Побочные действия, возникающие на
фоне комбинированной терапии проспидином и метотрексатом являются в основном
доброкачественными, проходят самостоятельно, не требуют дополнительной коррекции
и встречаются у 33,3% больных. Частота отмен из-за лекарственной токсичности не
превышает 18,6%.
5.
Комбинированная терапия проспидином и метотрексатом у больных РА, по
сравнению с монотерапией метотрексатом, оказывает более быстрое (стационарный
этап лечения) и выраженное положительное влияние на функциональный статус,
качество жизни и позволяет сдерживать темпы рентгенологического
прогрессирования через 12-36 месяцев непрерывной терапии. Переход в более
тяжелую стадию на фоне комбинированной терапии проспидином и метотрексатом
отмечается у 5,3% больных.
6.
Комбинированная терапия проспидином и метотрексатом оказывает более
выраженный клинический эффект у больных ранним РА, по сравнению с больными со
стажем болезни более 1 года (улучшение
ACR
50% и 70% отмечено у 82,6% и 45,2% больных, р=0,008; ремиссия - у 25% и 14,9%
соответственно).
7.
Применение комбинированной терапии проспидином и метотрексатом у больных
ранним РА, по сравнению с монотерапией метотрексатом, оказывает более быстрый и
выраженный клинический эффект (улучшение
ACR
50% и 70% на стационарном этапе наблюдается у 85,7% и 11,4% больных
соответственно, р=0,001), чаще приводит к снижению суточной потребности в НПВС и
ГКС (в случае стероидозависимости) и ремиссии заболевания (25% и 14,3%
соответственно), замедляет темпы рентгенологического прогрессирования.
8.
Комбинированная терапия проспидином и метотрексатом у больных ПсА, по
сравнению с монотерапией метотрексатом, оказывает более ранний (на стационарном
этапе лечения) и выраженный клинический эффект (улучшение по
PsARC
наблюдается у 71,4% и 16,1% больных к 1 месяцу лечения, р=0,001; у 64% и 54,5%
больных к 12 месяцу терапии соответственно), чаще приводит к ремиссии
заболевания (23,3% и 9,1% соответственно), снижению суточной потребности в НПВС.
9.
Побочные действия, возникающие в процессе применения комбинированной
терапии проспидином и метотрексатом при ПсА, являются в основном
доброкачественными, проходят самостоятельно, не требуют дополнительной коррекции
и встречаются у 23,3% больных. Частота отмены терапии в связи с побочными
действиями не превышает 10%.
10.
По результатам сравнительного контролируемого исследования
комбинированная терапия проспидином и метотрексатом у больных ПсА, по сравнению
с монотерапией метотрексатом, замедляет темпы рентгенологического
прогрессирования и оказывает более выраженное положительное влияние на
функциональный статус и качество жизни больных. Переход в более тяжелую стадию
на фоне комбинированной терапии проспидином и метотрексатом отмечается у 6,7%
больных.
11.
Проведенное исследование позволило
разработать рациональную методику применения комбинированной терапии проспидином
и метотрексатом при РА и ПсА, включающую дозы и интервал введения препаратов на
стационарном этапе и в процессе поддерживающей терапии.
12.
Высокая клиническая эффективность и
достаточно хорошая переносимость комбинированной терапии проспидином и
метотрексатом позволяют рассматривать эту комбинацию в качестве средства выбора
в терапии неблагоприятных вариантов РА и ПсА.
ПРАКТИЧЕСКИЕ РЕКОМЕНДАЦИИ
1.
Показаниями к применению комбинированной терапии проспидином и
метотрексатом являются достоверный диагноз РА и ПсА,
II-III
степени активности, наличие экстраартикулярных проявлений, резистентность к
другим видам базисной терапии или ее непереносимость.
2.
Комбинированную терапию проспидином и метотрексатом рекомендуется
начинать в условиях стационара после предварительного дообследования для
исключения противопоказаний и определения индивидуальной чувствительности к
проспидину путем введения пробной дозы 50 мг проспидина растворенного 2,5 мл
физиологического раствора внутримышечно.
3.
Режим дозирования в стационаре. При хорошей переносимости проспидина, его
назначают в дозе 200-300 мг внутривенно капельно медленно на 200,0 мл 5%
раствора глюкозы 1 раз в неделю. Выбор дозы проспидина зависит от активности
болезни переносимости препарата (при
II
степени активности назначается 200 мг 1 раз в неделю, при
III
степени активности назначается 300 мг 1 раз в неделю). На 3 сутки после введения
проспидина назначается метотрексат в дозе 10 мг внутримышечно 1 раз в неделю.
Всего на стационарном этапе проводят 4-5 таких комбинированных введений.
4.
Поддерживающая терапия. Методика поддерживающей терапии выбирается
индивидуально и зависит от результатов стационарного этапа лечения. На
амбулаторно-поликлиническом этапе рекомендуется вводить проспидин в дозе 100-200
мг внутримышечно 1 раз в неделю, а доза метотрексата остается прежней 10 мг в
неделю на 3 сутки после введения проспидина. Поддерживающая терапия
осуществляется в течение 6-12-36 месяцев. При появлении признаков нарастания
активности дозу проспидина увеличивают до 200-300 мг в неделю, доза метотрексата
остается 10 мг в неделю и проводится локальная терапия. При условии хорошего
эффекта от проводимой терапии и минимальной активности болезни проспидин
рекомендуется делать в дозе 100 мг, увеличивая интервал до 2 недель, доза и
режим введения метотрексата не изменяется, и составляет 10 мг в неделю
внутримышечно.
5.
Лабораторными показателями для назначения комбинированной терапии
проспидином и метотрексатом и контролем за ее эффективностью могут служить
высокие титры РФ, СРБ, уровень иммуноглобулинов основных классов и ЦИК, из
специальных дополнительных методов – повышения уровня стабильных метаболитов
оксида азота сыворотки крови и мочи. Лабораторными методами контроля за
возможными побочными действиями комбинированной терапии проспидином и
метотрексатом являются: общий анализ крови с тромбоцитами, определение уровня
билирубина и печеночных ферментов АлТ, АсТ, определение уровня мочевины,
креатинина сыворотки крови, общий анализ мочи.
6.
В процессе терапии необходимо контролировать побочные действия
комбинированной терапии проспидином и метотрексатом, которые проявляются в
основном парестезиями, повышенной чувствительностью к холоду, преходящими
нарушениями менструального цикла, умеренным повышением активности печеночных
ферментов, диспептическими и дизурическими явлениями, умеренной протеинурией.
Эти побочные действия носят, как правило, преходящий характер и проходят
самостоятельно при уменьшении дозы препаратов или увеличения интервала между
введениями препаратов. Появление аллергического дерматита и тяжелых церебральных
расстройств требует отмены препаратов. Во время внутривенного введения
проспидина возможно появление чувства жара, легкого головокружения, приливов к
лицу. Эти ощущения кратковременны, проходят самостоятельно и легче переносятся
больными при введении препарата в положении лежа.
7.
Противопоказаниями к назначению комбинированной терапии проспидином и
метотрексатом являются: индивидуальная непереносимость препаратов, нарушение
функции почек, печени, беременность, период лактации, тяжелые сопутствующие
заболевания внутренних органов с функциональной недостаточностью, сахарный
диабет, цереброваскулярная недостаточность, инфекционные заболевания.
Список работ, опубликованных по теме диссертации.
1. Немцов Б.Ф., Тимина О.В. Сравнительная характеристика побочных действий
цитостатических средств при ревматоидном артрите. Материалы научной конференции
НИИ гематологии и переливания крови. Актуальные вопросы трансфузиологии и
клинической медицины. Киров;
1995: 75-76.
2. Benenson
Е.,
Timina O., Bohlen H., Diehl V. Methotrexate versus prospidine pulse in
rheumatoid arthritis: effects on proliferation and activation of B cells. The
official EULAR journal for education and information: Rheumatology in Europe.
Supp. № 3, v24, 1995, 18th European Congress of Rheumatology. Abstracts.
Amsterdam. The Netherlands; 1995. D.77.
3. Benenson E., Timina O., Heiling
B., Diehl V. Prospidine versus Methotrexate in Rheumatoid Arthritis: a
controlled 12-month clinical trials. IX Symposium Eular 96. Rheumatology in
Europe. 1996; 1 (25): 54.
4. Benenson E., Timina O., Heiling
B., Diehl V. Efficiency of Prospidine vs. Methotrexate in RA: a controlled
12-month clinical trial. Arthritis
&
Rheumatism, 1996; 9 (39). Abstracts. Suppl.
№ 459.
5. Немцов Б.Ф., Тимина О.В. Фармакотерапия
ревматоидного артрита. Методическое пособие. КГМИ., 1995, 35 с.
6.
Немцов Б.Ф., Тимина О.В. Пульс-терапия проспидином и циклофосфаном при
ревматоидном артрите. II Всероссийский съезд ревматологов. Тезисы. Тула; 1997:
136.
7.
Немцов Б.Ф., Тимина О.В. Сравнительный анализ двух способов применения
метотрексата при ревматоидном артрите. II Всероссийский съезд ревматологов.
Тезисы. Тула; 1997: 135.
8.
Бененсон Е.В,
Немцов Б.Ф.,
Тимина О.В.,
Диль В.,
Нелиг В.
Efficiency of Prospidine vs. Methotrexate in RA: a cont-rolled 12-month clinical
trial. II Всероссийский съезд
ревматологов. Тезисы.
Тула;
1997: 206.
9.
Benenson E., Timina O., Heiling B., Diehl V. Wirksamkeit von Prospidin vs MTX
bei Patienten mit Rheumatoid Arthritis. “Netwerk Rheumatologie” Regionaltagu-ng
der Deutschen Gesell-schaft fiir Rheuma-tologie. Dusseldorf;
1997: 20.
10. Немцов
Б.Ф., Тимина О.В., Смирнова Л.А. Клиническая оценка эффективности пульс-терапии
при системных заболеваниях соединительной ткани. Материалы научной конференции
Института ревматологии РАМН «Актуальные вопросы диагностики и лечения системных
заболеваний соединительной ткани». Тезисы. Москва; 1996: 13-14.
11. Немцов
Б.Ф., Тимина О.В. Сравнительная эффективность пульс-терапии проспидином и
метотрексатом при ревматоидном артрите (12-мес. контролируемое исследование).
“Клиническая медицина”. 1998; 8: 25-28.
12. Немцов Б.Ф., Тимина О.В. Случай
гепатоцеллюлярной карциномы у больной ювенильным ревматоидным артритом,
лечившейся цитостатиками. Российская ревматология. 1998; 3: 57-60.
13. Тимина О.В., Немцов Б.Ф. Сравнительная
эффективность пульс-терапии проспидином, метотрексатом и циклофосфаном при
ревматоидном артрите (12-месячное контролируемое исследование). Вятский
медицинский вестник; 1999; 2: 22-25.
14. Немцов Б.Ф., Смирнова Л.А., Тимина О.В.
Нарушение вибрационной чувствительности при ревматоидном артрите.
Научно–практическая ревматология. 2000; 1: 24-28.
15. Немцов Б.Ф., Тимина О.В. Стероидосберегающий
эффект базисных средств у больных ревматоидным артритом. Тезисы
научно-практической конференции “Современные аспекты глюкокортикостероидной
терапии ревматических заболеваний”. Москва. Российская ревматология. 1999: 74,
26-30 октября 1999.
16. Немцов Б.Ф., Тимина О.В. Внутрисуставное
применение проспидина при ревматоидном артрите. Юбилейная конференция,
посвященная 15-летию НИИ клинической и экспериментальной ревматологии РАМН.
Тезисы. Волгоград; 2000: 101.
17. Немцов Б.Ф., Тимина О.В. Иммунологические
эффекты пульс-терапии проспидином и метотрексатом при ревматоидном артрите.
Юбилейная конференция посвященная 15-летию НИИ клинической и экспериментальной
ревматологии РАМН. Тезисы. Волгоград; 2000: 101-102.
18. Немцов Б.Ф., Постникова Г.А., Симонова О.В.
Изучение содержания метаболитов оксида азота у больных ревматоидным артритом.
Тезисы конференции «Медико-социальные проблемы костно – мышечных заболеваний в
21 веке». Москва. Научно-практическая ревматология. 2000: 78-79.
19. Немцов Б.Ф., Симонова О.В., Политова Н.Н.
Комбинированная терапия проспидином и метотрексатом при ревматоидном артрите.
Предварительные результаты. Тезисы
III
съезда ревматологов. Рязань; 2001. 297.
20. Немцов Б.Ф., Симонова О.В., Политова Н.Н.
Сравнительный анализ эффективности базисной терапии ревматоидного артрита.
Материалы научной сессии КФ АЕ и ВРО РАЕН. Киров;
2001. 100-101.
21. E.
Вenenson,
B. Nemtzov, O. Simonova. Efficacy and safety of prospidine vs
methotrexate in active RA: results of a controlled, randomized 12-month
trial. 66th Annual Scientific Meeting American College of
Rheumatology. Abstracts. San Francisco; 2001.
1899.
22. B.F. Nemtsov, L.A. Smirnova,
O.V. Simonova. New approaches in diagnosis of sensor polyneuropathy in
RA. Abstracts Аnnual
European Congress of Rheumatology. Prague Czech Republic; 2001. THU0133.
119.
23. Немцов Б.Ф., Симонова О.В. Комбинированная
терапия проспидином и метотрексатом в терапии анкилозирующего спондилоартрита.
Предварительные результаты. Тезисы научно-практической конференции ревматологов
«Новое в диагностике и лечении ревматических болезней». Москва.
Научно-практическая ревматология. 2002; 4: 112.
24. Симонова О.В., Немцов Б.Ф., Сухих Е.Н.
Клинические особенности серонегативных спондилоартритов. Сборник научных работ
«Актуальные проблемы современной ревматологии». Волгоград; 2003: 113-114.
25. Симонова О.В., Немцов Б.Ф., Политова Н.Н.
Влияние комбинированной терапии проспидином и метотрексатом на
экстраартикулярные проявления ревматоидного артрита. Сборник научных работ
«Актуальные проблемы современной ревматологии». Волгоград; 2003: 114-115.
26. Немцов Б.Ф., Симонова О.В., Политова Н.Н., Бененсон Е.В.
Способ лечения ревматоидного артрита. Патент на изобретение №2199320 от
27.02.2003: 1-16.
27. Немцов Б.Ф., Симонова О.В., Политова Н.Н.,
Бененсон Е.В. Сравнительная оценка комбинированной терапии проспидином и
метотрексатом при ревматоидном артрите (отдаленные результаты). Тезисы
Конгресса ревматологов России. Саратов. Научно-практическая ревматология.
2003; приложение к №2: 76.
28. Немцов Б.Ф., Симонова О.В., Политова Н.Н.
Оценка качества жизни больных ревматоидным артритом при комбинированной терапии
проспидином и метотрексатом. Тезисы Конгресса ревматологов России. Саратов.
Научно-практическая ревматология. 2003; приложение к №2: с.76.
29. Политова Н.Н., Немцов Б.Ф., Симонова О.В.
Сравнительная характеристика побочных действий при применении комбинированной
терапии проспидином и метотрексатом и монотерапии метотрексатом при ревматоидном
артрите. Тезисы Конгресса ревматологов России. Саратов. Научно-практическая
ревматология. 2003; приложение к №2: 82.
30. B. Nemtzov, O. Simonova, N.
Politova, E. Вenenson.
Clinical efficacy of combination therapy of prospidine and methotrexate
vs monotherapy of methotrexate for Rheumatoid Arthritis.
Аnnual
European Congress of Rheumatology EULAR 2003. Abstracts. Lisbon.
Portugal; 2003. THU0193.
31. Немцов Б.Ф., Симонова О.В., Политова Н.Н., Бененсон Е.В.
Комбинированная терапия проспидином и метотрексатом у больных ревматоидным
артритом (12 месячное контролируемое исследование). Научно-практическая
ревматология. 2003; 3: 43-46.
32. Симонова О.В., Немцов Б.Ф. Эффективность и
переносимость базисной терапии у больных ревматоидным артритом пожилого
возраста. Материалы межрегиональной научно-практической конференции «Что мешает
жить пожилому человеку? Болезни суставов и сердца». Ярославль; 2003: 65-66.
33. Немцов Б.Ф., Симонова О.В. Влияние базисной
терапии на функциональный статус и качество жизни больных ревматоидным артритом
пожилого возраста. Материалы межрегиональной научно-практической конференции
«Что мешает жить пожилому человеку? Болезни суставов и сердца». Ярославль; 2003:
59-60.
34.
B.F.
Nemtsov,
O.V.
Simonova,
N.N.
Politova.
Clinical efficacy of
combination therapy of prospidin and methotrexate in patients with early
rheumatoid arthritis. Annual European Congress of Rheumatology. Abstracts.
Berlin, 9-12 June 2004, FRI0001.
35. O.V. Simonova, B.F. Nemtsov.
Combination therapy of prospidin and methotrexate for psoriatic arthritis.
Annual European Congress of Rheumatology. Abstracts. Berlin, 9-12 June 2004,
SAT0001.
36. Политова Н.Н., Симонова О.В., Немцов Б.Ф.
Комбинированная терапия ревматоидного артрита, резистентного к лечению
метотрексатом. Тезисы школы молодых ученых с конференцией «Актуальные вопросы
практической и теоретической ревматологии», Звенигород, 24-26 мая 2004.
Научно-практическая ревматология. 2004; 2: 138.
37. Немцов Б.Ф., Симонова О.В. Функциональный
статус и качество жизни у больных псориатическим артритом под влиянием
комбинированной терапии. Тезисы научно-практической конференции «Социальные
аспекты ревматических болезней». Москва, 27-28 мая, 2004. Научно-практическая
ревматология. 2004; 2: 83.
38. Симонова О.В., Немцов Б.Ф. Функциональный
статус и качество жизни при раннем ревматоидном артрите в процессе
комбинированной терапии. Тезисы научно-практической конференции «Социальные
аспекты ревматических болезней» Москва, 27-28 мая, 2004. Научно-практическая
ревматология. 2004; 2: 86.
39. Симонова О.В., Немцов Б.Ф. Влияние
комбинированной терапии на показатели стабильных метаболитов оксида азота у
больных псориатическим артритом. Сборник научных работ «Актуальные проблемы
современной ревматологии и кардиологии». Волгоград, 2004: 102-103.
40. Немцов Б.Ф., Симонова О.В. Эффективность
комбинированной терапии проспидином и метотрексатом и комбинации метотрексата и
низких доз преднизолона при ревматоидном артрите. Сборник научных работ
«Актуальные проблемы современной ревматологии и кардиологии». Волгоград, 2004:
81-82.
41. Симонова О.В., Немцов Б.Ф. Клиническая
эффективность комбинированной терапии проспидином и метотрексатом и монотерапии
проспидином у больных ревматоидным артритом. Сборник научных работ «Актуальные
проблемы современной ревматологии и кардиологии». Волгоград, 2004: 103-104.
42. Симонова
О.В., Немцов Б.Ф. Комбинированная терапия метотрексатом и преднизолоном при
ревматоидном артрите. Казанский медицинский журнал. 2004; 4: 245-248.
43. Симонова
О.В., Немцов Б.Ф., Политова Н.Н. Влияние комбинированной терапии проспидином и
метотрексатом на рентгенологическое прогрессирование, функциональный статус и
качество жизни больных ревматоидным артритом. Научно-практическая ревматология.
2004; 3: 25-30.
44. Симонова О.В., Немцов Б.Ф., Политова Н.Н. Комбинированная
терапия ревматоидного артрита, резистентного к терапии метотрексатом.
Нижегородский медицинский журнал. 2004; 2: 57-62.
45. Немцов
Б.Ф., Симонова О.В. Способ лечения псориатического артрита. Патент на
изобретение №2228755 от 20.05.2004: 1-14. |
