МЕХАНИЗМЫ ДЕЙСТВИЯ
Химико-фармацевтический
журнал, 1976, № 12, стр. 7 - 13
О РОЛИ
ПЛАЗМАТИЧЕСКОЙ МЕМБРАНЫ В МЕХАНИЗМЕ ПРОТИВООПУХОЛЕВОГО ДЕЙСТВИЯ ПРОСПИДИНА
В. А. Чернов, С. В. Геодакян
Проспидин — дихлорид
N,N'"-ди(γ-хлор-β-оксипропил)-
N,N'"-диспиротрипиперазиния
(I) — относится к новой группе химических соединений — производным
диспиротрипиперазиния. Обладая высокой противоопухолевой активностью, он
отличается от известных противоопухолевых препаратов малой токсичностью, большой
терапевтической широтой действия, отсутствием угнетающего действия на
кроветворение [1, 2].
Механизм действия проспидина до сих пор еще
недостаточно ясен. Ранее были проведены исследования, в которых проверялось
наличие у проспидина аспектов механизма действия, характерных для других
противоопухолевых препаратов. При этом оказалось, что проспидин по влиянию на
внутриклеточные процессы отличается от цитостатических веществ из группы
алкилирующих агентов. Так, при введении проспидина крысам с саркомой 45 не
обнаружено [31 различий в количестве ДНК в ядрах опухолевых клеток по сравнению
с контролем, в то время как, например, сарколизин уменьшает количество ДНК и РНК
в клетке [4]. В наших опытах in
virto
в отличие от алкилирующих агентов вязкость
растворов ДНК тимуса теленка не изменялась при действии проспидина. Н. С.
Богомолова и В. А. Чернов [5] изучали влияние проспидина на аэробный и
анаэробный гликолиз и дыхание клеток асцитной опухоли Эрлиха (АОЭ) в аппарате
Варбурга. In
virto
при 20° проспидин не влиял на эти процессы,
in
vivo
его действие принципиально отличалось от
действия алкилирующего агента фосфемида. В сходных опытах
in
virto,
проведенных нами на клетках АОЭ при использовании полярографического метода,
также не было обнаружено различий в интенсивности дыхания клеток при воздействии
проспидином в концентрации 10-2 М.
Проспидин в терапевтических дозах не изменяет активность растворимой АТФ-азы в
опухоли, селезенке и тимусе крыс с саркомой 45, тогда как дипин ее увеличивает
[6, 7]. В отличие от алкилирующего агента дипина проспидин не изменяет
продолжительности фаз митотического цикла гепатоцитов регенерирующей печени
мышей после частичной гепатэктомии [8].
Указанные различия во влиянии проспидина на
внутриклеточные процессы в сравнении с другими препаратами обусловлены,
по-видимому, иным механизмом его действия на опухолевую клетку. Учитывая наличие
в молекуле проспидина четвертичных атомов азота и меньшую способность подобных
веществ по сравнению с третичными аминами проникать через некоторые
биологические мембраны (например, холинолитических веществ через
гемато-энцефалический барьер [9]), можно полагать, что в механизме
противоопухолевого действия проспидина немаловажное значение имеет
взаимодействие его с плазматической мембраной, которая, как известно, принимает
важное, если не первостепенное, участие в регуляции деления клетки [10, 11].
В связи с этим в опытах
in
virto
с помощью биофизических методов мы изучали
влияние проспидина на ионную проницаемость плазматической мембраны опухолевых
(клетки АОЭ мышей) и нормальных (эритроциты крыс) клеток. Из-за невозможности
подобрать нормальную ткань, гомологичную асцитному .раку Эрлиха (в настоящее
время данный штамм следует рассматривать как недифференцированную бластому), мы
остановили свой выбор на эритроцитах. Эритроцит, как известно, лишен
внутриклеточных мембран и органелл, поэтому действие вещества на осмотический
гемолиз можно с большей вероятностью отнести за счет действия его на мембрану.
Для сравнения одновременно с проспидином в аналогичных опытах изучали влияние на
проницаемость плазматической мембраны четырех противоопухолевых препаратов из
группы алкилирующих агентов — дипина (III), фопурина (IV), фосфемида (V) и
фотрина (VI), а также аналога проспидина (II), не обладающего антибластической
активностью.

Экспериментальная часть
Для изучения влияния препаратов на проницаемость
плазматической мембраны опухолевых клеток использовали асцит, взятый из брюшной
полости мышей с АОЭ на 10—12-й день после перевивки. Асцит разводили средой 199
(1 : 3) и центрифугировали при 1000
g в
течение 5 мин. Надосадочную жидкость сливали и осадок дважды отмывали средой
199, после чего готовили суспензию клеток и выдерживали ее в течение 2 ч при
комнатной температуре. Затем клетки осаждали центрифугированием при 3000
g
в течение 5 мин и осадок использовали в опытах,
которые были проведены в двух сериях. В одной серии опытов из осадка готовили
10% суспензию клеток в растворе 0,3 М сахарозы в 0,01 М трис-НСl
буферном растворе (рН 7,5) с предварительно растворенным в нем испытуемым
веществом в различных концентрациях. В качестве контроля использовали суспензию,
приготовленную в среде без препарата. В начальный момент времени и спустя 1 ч из
опытной и контрольной суспензий брали пробы для определения объемной
концентрации клеток, электропроводности внеклеточной жидкости и концентрации в
ней К+ и Nа+. Внеклеточную жидкость получали
центрифугированием суспензии при 3000
g
в течение 5 мин. Результаты измерений выражали
в процентах по отношению к контролю.
В другой серии опытов опухолевые клетки предварительно
инкубировали с испытуемым веществом в среде 199 при комнатной температуре в
течение 2 ч и осаждали их центрифугированием при 3000
g
в течение 5 мин. Из осадка готовили 10%
клеточную суспензию на малоионной среде следующего состава: 40% среды 199 и 60%
сахарозы и добавляли детергент тритон Х-100 в различных концентрациях. Контролем
служила суспензия, приготовленная из клеток, инкубированных без препарата. В
начальный момент времени и через 1 ч измеряли электропроводность опытной и
контрольной суспензий, результаты выражали графически.
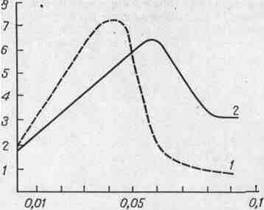
Рис. 1.
Изменение проспидином повреждающего действия неионного детергента тритона Х-100
на плазматическую мембрану клеток АОЭ.
I
— детергент; 2 — проспидин + детергент.
По оси ординат — изменение
электропроводности через 1 ч (x10
-4 Ом-1
x см-1);
по оси абсцисс — концентрация
тритона Х-100 (в %).
На графике вычерчивалась кривая, выражающая
зависимость изменения электропроводности суспензии через 1 ч от концентрации
детергента (рис. 1). Левая часть кривой отражает выход ионов под влиянием
детергента, правая —лизис клеток. Указанные среды (сахароза с трис-буфером,
среда 199 с сахарозой) и сроки (продолжительность инкубации суспензии и интервал
между измерениями) явились оптимальными для решения поставленных задач и были
выбраны нами в предварительных опытах. В упомянутых средах разность концентраций
ионов внутри и снаружи клеток, а также проницаемость поверхностной мембраны
больше, чем в среде 199, и отчетливее проявляется влияние препарата и
повреждающее действие детергента на мембрану. Электропроводность суспензии
определяли на сконструированной нами автоматизированной кондуктометрической
установке с четырехэлектродными ячейками на частоте 10 кГц, электропроводность
внеклеточной жидкости — на мосте переменного тока Р-568 с двухэлектродной
ячейкой. Концентрацию ионов К+ и
Na+
измеряли на пламенном фотометре ФПЛ-1. Об объеме опухолевых клеток судили по их
объемной концентрации в суспензии, определяемой с помощью гематокритной
микроцентрифуги МЦГ-8. Суспензию центрифугировали при 4600
g в
течение 5 мин.
Для изучения действия препаратов на мембрану
эритроцитов мы использовали кровь крыс самцов. Крысу декапитировали, кровь
собирали в стакан, содержащий 5 мл смеси фосфатного буферного раствора (рH
7,5) и 3,7% раствора цитрата натрия (9 : 1), и центрифугировали в течение 10 мин
при 1000 g.
Осажденные эритроциты 3 раза отмывали фосфатным буферным раствором и готовили
суспензию, содержащую 5,0±0,3-107 клеток в 1 мл. Сливали равные
объемы суспензии эритроцитов и раствора препарата в фосфатном буферном растворе
(в контрольную суспензию добавляли фосфатный буферный раствор без препарата) и
инкубировали в течение 1 ч при 37°. Указанное время инкубации было оптимальным
для проявления эффекта препаратов, что установлено в предварительных опытах, в
которых инкубацию эритроцитов с препаратом проводили в течение 3 ч. О действии
веществ на плазматическую мембрану эритроцитов судили по интенсивности гемолиза,
который вызывали, добавляя к 0,5 мл инкубационной смеси (опытной и контрольной)
4,5 мл фосфатного буферного раствора, разбавленного дистиллированной водой. При
смешивании 0,5 мл суспензии с 4,5 мл фосфатного буферного раствора,
разбавленного в 2,3 раза, в контрольной суспензии происходил 50% гемолиз
эритроцитов. После разбавления суспензию выдерживали 5 мин при комнатной
температуре, затем для прекращения гемолиза добавляли 1 мл 1 М раствора
сахарозы, центрифугировали в течение 5 мин при 3000
g и
определяли оптическую плотность гемоглобина в супернатанте при 418 нм на
спектрофотометре СФ-4. Отношение оптической плотности в опытном растворе к
оптической плотности в контроле давало величину относительного гемолиза.
Использованные нами в опытах проспидин, дипин, фотрин,
фопурин и фосфемид, а также неактивный аналог проспидина (II) синтезированы во
Всесоюзном химико-фармацевтическом институте им. С. Орджоникидзе; тритон
Х-100 — фирмы «Ferak».
Цифровые данные опытов обрабатывали статистически, применяя известные методы
[12].
Результаты опытов и их обсуждение
О влиянии проспидина, его неактивного аналога и
алкилирующих агентов — дипина, фотрина, фопурина и фосфемида на проницаемость
поверхностной мембраны опухолевых клеток АОЭ можно судить по изменению
клеточного объема, электропроводности внеклеточной среды, а также по
концентрации в ней К+ и
Na+
(см. таблицу, рис. 2).
Изменение объемной концентрации клеток АОЭ в
суспензии электропроводности внеклеточной среды и концентрации в ней К+
и Na+
при действии проспидина дипина и фотрина
|
Препарат |
Концентрация препарата, М |
Объемная концентрация клеток |
Электропроводность среды |
Концентрация в среде
ионов |
|
К+ |
Na+ |
|
Проспидин |
10-2 |
- 53 |
- 47 |
- 8 |
- 15 |
|
10-3 |
0 |
- 14 |
- 24 |
- 23 |
|
10-4 |
+ 5 |
+ 11 |
+ 6 |
- 3 |
|
Дипин |
10-2 |
+ 15 |
- 30 |
- 15 |
- 3 |
|
10-3 |
0 |
0 |
+ 27 |
- 20 |
|
10-4 |
0 |
0 |
+ 20 |
0 |
|
Фотрин |
10-2 |
+ 15 |
- 6 |
+ 6 |
- 26 |
|
10-3 |
0 |
0 |
0 |
0 |
|
10-4 |
0 |
0 |
0 |
0 |
Примечание. Все величины даны в
процентах по отношению к контролю; плюс — увеличение; минус — уменьшение; ноль —
нет эффекта.
Дипин увеличивает объемную концентрацию клеток и
вытекание ионов калия и уменьшает выход натрия. Суммарное вытекание ионов из
клетки уменьшается. Эти данные указывают на нарушение плазматической мембраны
клеток АОЭ. Сходное действие на клеточный объем и суммарную проницаемость
клеточной мембраны для ионов оказали фотрин, фопурин и фосфемид. Фотрин и
фопурин влияли на выход К+ и
Na+
аналогично дипину, но в меньшей степени. Изучение фосфемида на вытекание К+
и Na+
было проведено в ограниченном числе опытов, в которых отмечено некоторое
уменьшение выхода К+ и увеличение выхода
Na+.
Еще большее повреждение плазматической мембраны клеток АОЭ отмечалось при
применении неактивного аналога проспидина (II): наблюдалось значительное
увеличение клеточного объема, суммарного вытекания ионов и выхода К+
при ослаблении перемещения Na+.
Принципиально иные результаты получены с проспидином, который значительно
уменьшает клеточный объем и вытекание из клеток и К+, и Nа+.
Суммарное перемещение ионов в клеточной суспензии в присутствии проспидина также
значительно замедляется.
Итак, если противоопухолевые препараты из группы
алкилирующих агентов —дипин, фотрин, фопурин и фосфемид, а также неактивный
аналог проспидина приводят к повреждению клеточной поверхности, то применение
проспидина, напротив, сопровождается ее стабилизацией. В этой связи известный
интерес представляют данные о способности проспидина «защищать» клетки АОЭ от
повреждающего действия неионного детергента тритона Х—100. На это указывает
сдвиг кривой изменения электропроводности суспензии клеток АОЭ (предварительно
инкубированных с проспидином в течение 2 ч в концентрации 10-2М) в
сторону больших концентраций детергента (см. рис. 1). При помещении же
опухолевых клеток (предварительно инкубированных с препаратом) в сахарозу без
детергента электропроводность полученной суспензии не отличалась от
электропроводности в контроле. Следовательно, можно полагать, что проспидин
стабилизирует те участки мембраны, на которые действует детергент.

Рис. 2. Изменение электропроводности
внеклеточной среды (столбики) и объемной концентрации (окружности) в суспензии
клеток АОЭ при действии проспидина и других веществ в концентрации 10-2
М.
Таким образом, и по действию на плазматическую
мембрану опухолевых клеток (АОЭ) проспидин существенно отличается от других
противоопухолевых препаратов из группы алкилирующих агентов. Однако это отличие
само по себе еще не может служить основанием для того, чтобы говорить о ведущей
роли плазматической мембраны опухолевых клеток в механизме противоопухолевого
действия проспидина. Для этого необходимо также знать, каким образом реагирует
на действие этого препарата мембрана нормальной клетки. Этот вопрос мы пытались
решить во второй серии опытов, проведенных на эритроцитах крыс. Оказалось, что в
отличие от опухолевых клеток проспидин в тех же концентрациях оказывает на
эритроцитную мембрану слабое повреждающее действие (рис. 3). В этом отношении он
ведет себя подобно фотрину. Дипин не влияет, а фопурин оказывает на эритроцитную
мембрану стабилизирующее действие. Следовательно, по действию на мембрану
эритроцитов проспидин мало чем отличается от алкилирующих агентов. Более того, с
фопурином он как бы поменялся местами: фопурин оказывает на эритроцитную
мембрану такое же стабилизирующее действие, какое проспидин на плазматическую
мембрану клеток АОЭ. Обобщая результаты опытов обеих серий, можно полагать, что
в механизме противоопухолевого действия проспидина немаловажная роль принадлежит
плазматической мембране.
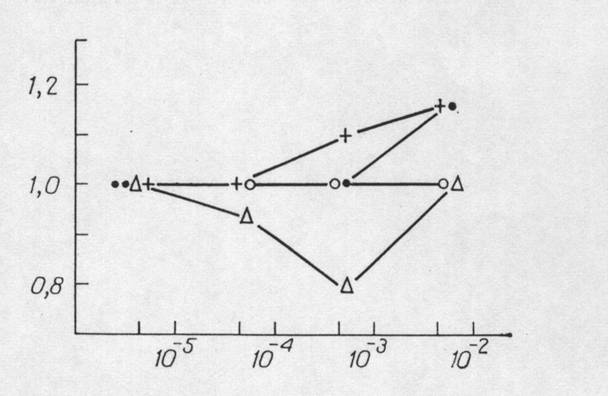
Рис. 3. Действие проспидина, дипина,
фотрина и фопурина на гемолиз эритроцитов.
○ –
III;
∆ - IV;
● –
I;
+ - VI.
По оси ординат — относительная
величина гемолиза (по сравнению с контролем); по оси абсцисс — конечная
концентрация препарата (в М).
С этих позиций представляют большой интерес результаты
опытов в которых выясняли значение некоторых структурных элементов молекулы
этого соединения для противоопухолевой активности и, в частности, роль галогена
в γ-хлор-β-оксипропильных группах и диспиротрипиперазиниевой системы, имеющей
два четвертичных атома азота [13]. Было установлено, что соединения, содержащие
в отличие от проспидина в γ-положении концевых группировок алкиламинные остатки,
не обладали антибластической активностью. Оказалось, что наличие двух
четвертичных атомов азота в диспиротрипиперазиниевой системе является важным
условием для противоопухолевой активности проспидина. Этот вывод вытекает, в
частности, из сопоставления его аналогов, имеющих по два четвертичных атома
азота с соответствующими соединениями, не являющимися четвертичными аммониевыми
солями. Соединения первой группы обладают активностью, а второй — ее лишены.
Интересно, что противоопухолевая активность соединений зависит от числа
метиленовых звеньев между пиперазиниевыми циклами. Аналогичная закономерность
наблюдается и при возрастании числа циклов (от 1 до 5). Максимальной
противоопухолевой активностью и минимальной токсичностью обладало соединение с
трехциклической структурой [2]. Все эти факты указывают на важную роль
расстояния между активными центрами молекулы проспидина и его аналогов в
способности избирательно нарушать жизнедеятельность опухолевых клеток по
сравнению с нормальными.
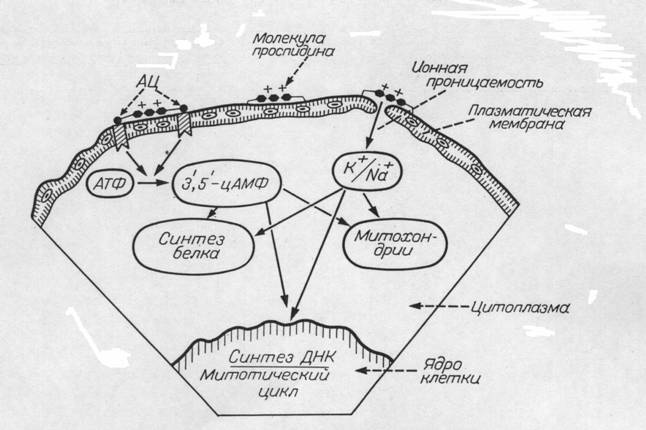
Рис. 4. Возможные
пути влияния проспидина на внутриклеточные процессы через плазматическую
мембрану.
Принимая во внимание данные литературы и результаты
наших опытов, мы полагаем, что ведущим звеном в механизме действия проспидина на
опухолевую клетку следует считать изменения, вызываемые препаратом в ее
плазматической мембране. Не исключено при этом, что молекула проспидина вообще
не проникает в клетку. Нам представляются наиболее вероятными два пути
воздействия проспидина на внутриклеточные процессы через клеточную поверхность
(рис. 4). Первый путь —это воздействие на ионный гомеостаз (ИГ) клетки, так как
даже кратковременные влияния на систему ИГ могут вести к существенным изменениям
в функции и делении клеток [14]. О влиянии проспидина на ИГ клеток АОЭ
свидетельствует уменьшение вытекания К+ и
Na+,
что приводит к нарушению абсолютных концентраций ионов в клетке. Подобное
изменение в ионной проницаемости мембраны может нарушать нормальное отношение К+
/Na+
. Как известно, от абсолютных концентраций ионов калия и натрия в клетке и от их
соотношения зависит активность многих ферментов [15], биосинтез ДНК и развитие
других процессов в клетках [16, 17]. Возможен и другой путь. Влияние проспидина
на внутриклеточные процессы опосредуется участками клеточной мембраны, которыми
могут оказаться рецепторные зоны, включающие встроенные в мембрану молекулы
ферментов. С этой точки зрения наибольший интерес представляет аденилатциклаза (АЦ)
— фермент, катализирующий образование циклического аденозин-3',5'-монофосфата из
АТФ [18]. Участие АЦ в осуществлении влияния на внутриклеточные процессы
показано на примере некоторых гормонов. Изменение активности АЦ, вызываемое
гормоном с поверхности клетки, отражается на концентрации циклического АМФ,
играющего роль внутриклеточного медиатора в воздействии на метаболические
процессы и деление клеток [19]. Не исключено, что и влияние проспидина на
жизнедеятельность опухолевых клеток осуществляется через АЦ.
Ранее была показана
зависимость активности проспидина и его аналогов от расстояния между
реакционноспособными центрами в их молекуле. Весьма вероятно, что это расстояние
соответствует расстоянию между рецепторными зонами на поверхности опухолевых
клеток и не совпадает с ним в нормальных. Конечно, это предположение окажется
справедливым лишь при условии, если расстояния между рецепторами в опухолевых и
нормальных клетках различны. Косвенное подтверждение возможности действия
проспидина через эту систему дают также данные, приведенные в работе [20], в
которой показана возможность для бифункциональных алкилирующих агентов изменять
концентрацию циклического АМФ в клетке. С позиций мембранного механизма, как нам
представляется, можно объяснить некоторые особенности в фармакологических
свойствах проспидина (например, отсутствие угнетения гемопоэза) и упомянутые
выше отличия проспидина от других противоопухолевых препаратов в действии на
ДНК, энергетические процессы, клеточный цикл и т. д.
Л И Т Е РА Т У Р А.
1. Чернов В. А., Соркина Ю. А., Минакова С.М. — В кн.:
Проспидин — новое противоопухолевое средство. М., 1973, с. 23. — 28
2. Михалев В. А., Чернов В. А. — Там же, с. 6. — 10
3. Насыбуллин Р. А. К вопросу о значении гипофиза и
щитовидной железы в противоопухолевом действии проспидина. Автореф. дис. канд.
М., 1973.
4. Зовите В. Ф. и др.—«Труды АН Литовок. ССР. Сер. В», 1972,
т. 2, № 58, с. 123.
5. Богомолова Н. С., Чернов В. А.— В кн.: Проспидин—новое
противоопухолевое средство. М., 1973, с. 74.
6. Преснова Ж.Ф., Чернов В. А. — Там же, с. 78.
7. Они же. — «Фармакол. и токсикол.», 1968, № 4, с. 473.
8. Фактор В. М., Соколова А. С., Урываева И. В. и др. —
«Хим.-фарм. ж.», 1976, № 8, с. 20.
9. Михельсон М. Я., Саватеев Н. В., РожковаЕ.К. и др. — В
кн.: Физиологическая роль ацетилхолина и изыскание новых лекарственных веществ.
Л., 1957, с. 25.
10. Васильев Ю. М., Маленков А. Г. Клеточная поверхность и
реакции клеток. Л., 1968.
11. Pardee A. B. «In vitro», 1971, 7, N 2, c. 95.
12. Бейли Н. Статистические методы в биологии. М., 1963.
13. Дорохова М. И., Чернов В. А., Минакова С. М. и др. —
«Хим.-фарм. ж.», 1976, №2, с. 36.
14. Кафиани К. А., Маленков А. Г. — «Успехи совр. биол.»,
1976, т. 81, № 3, с. 445.
15. Диксн М., Уэбб Э. Ферменты. М.,
1965, с.
429.
16. Lubin M. — «Nature», 1967, v. 213, p. 451.
17. We11en J. J., Bencard Th. H. — «Biochim. biophys. Acta»,
1969, v. 183, p. 110.
18. Suther1and E. W., Ra11T. W. — «Pharmacol. Rev.»,
1960, V. 12, p. 265.
19. Suther1and E. W. — «Science», 1972, v. 177, p. 401.
20. Tisda1e M. J., Phi11ips B. J.— «Biochem. PharmacoU, 1975, v. 24, p. 211.
|
